Что делать при отеке руки после химиотерапии

Отеки — частое осложнение распространенного рака, кроме того у любого онкологического больного могут быть и другие причины для развития отечного синдрома, существенно усугубляющие состояние и усиливающие отечность тканей. Особенность отеков при раке в их устойчивости к лечению и нередкое тяжелое течение с выраженным болевым синдромом.
Виды отёков при раке
Отеки при раке, а точнее отечный синдром, обусловленный выходом жидкости из сосудистого русла и длительной задержкой в тканях, может быть симметричным или генерализованным и локальным, с преимущественным поражением отдельной анатомической части.
К генерализованному варианту относится скопление жидкости во внутренних полостях организма — асцит или плеврит, а также перикардит — жидкость в сердечной сорочке.
Такое тяжелое и характерное для терминальных сердечных заболеваний состояние общей отечности организма, как анасарка, при раке встречается нечасто, тем не менее при раковой кахексии жировая клетчатка больного раком способна незаметно впитать до 5 литров «лишней» жидкости, формируя скрытый отечный синдром. У человека без истощения можно заметить избыточное скопление уже 2 литров межтканевой жидкости, при распространенном раке и сниженной активности заметить увеличение объема весьма непросто.
Локальные отеки при злокачественных процессах практически всегда не воспалительного характера, а обусловлены блокировкой оттока межтканевой жидкости по лимфатическим сосудам.
Причины отёков при раке
Отечность формируется при разбалансировке процесса выхода питающей клетки плазмы из кровеносного русла в ткани, откуда она почти полностью, но уже в «отработанном виде», должна всасываться венозными капиллярами. В норме только десятая часть жидкости задерживается в межклеточном пространстве и впоследствии уходит в лимфатическое русло.
При большинстве злокачественных процессов баланс нарушает недостаточное функционирование лимфатического коллектора, когда сосуды и лимфоузлы забиваются клетками рака, а опухолевые конгломераты лимфатических узлов перестают «качать» лимфу. Подобный механизм формирования отечности вплоть до слоновости возникает при неоперабельном раке шейки матки с метастазами в паховые и тазовые лимфоузлы. Аналогичное происходит при оперированном раке молочной железы с лимфедемой — лимфостазом, когда полностью удаляются подмышечные лимфоузлы, и при неоперабельном раке груди с метастатическими регионарными лимфоузлами, не только не функционирующими, но и дополнительно сдавливающими крупные сосуды.
Часто лимфатическую недостаточность усугубляет сдавление вены конгломератом опухолевых лимфоузлов и её тромбоз — сопряженное с распространенным злокачественным процессом нарушение свертывающей системы крови. Резко выраженный отек головы и шеи развивается при синдроме верхней полой вены, когда нарушает венозный отток быстро растущая в средостении злокачественная опухоль. Аналогичный механизм включается при поражении печени метастазами рака и увеличении органа до гигантского размера — во всю брюшную полость.
Нечасто встречающаяся паранеопластическая нефропатия, сопровождающая развитие злокачественного процесса с высокой потребностью в белке L-аспарагине, напрямую повреждает почечные клубочки, что ведет к потерям белков и развитию генерализованных отеков.
Механизм отёка при раковом истощении
При кахексии у онкологических пациентов механизм формирования «голодных» отеков обусловлен снижением концентрации циркулирующих в крови белков. Гипопротеинемия приводит к массированному выходу плазмы в межклеточное пространство, что автоматически сопровождается снижением артериального давления и, в свою очередь, включением компенсаторного механизма его повышения. Повышение сосудистого давления опять ведет к выведению жидкой части крови в интерстициальное пространство и ещё большей отечности тканей. Подобным образом формируются отеки при заболеваниях почек, осложненных почечной недостаточностью, циррозе печени с исходом в печеночную недостаточность.
В терминальной стадии рака недостаточность питания пациента сопряжена с падением функциональных возможностей печеночных клеток, не синтезирующих достаточного количества белков, и дополняется высочайшей потребностью раковых клеток в энергии за счёт «обкрадывания» всех остальных тканей организма. То есть формируется порочный круг, когда при недостаточном печеночном синтезе и низком поступлении извне белок усилено сжигается клетками рака.
Избыток жидкости в тканях при недостатке объема циркулирующей плазмы вынуждает организм к выбросу гормонов и биологически активных веществ, поддерживающих артериальное давление, что ещё больше подрывает сердечно-сосудистую и дыхательную систему, ухудшая состояние больного раком.
Скрытые отеки и анасарка при раковой кахексии требуют активных лечебных мероприятий, только капельницами с белковыми растворами удалить их невозможно. Необходимы активные и незамедлительные действия по купированию патологических реакций, которые специалисты Клиники выполняют по индивидуально разработанной и патогенетически ориентированной лечебной программе.
Диагностика и клинические симптомы
При раке диагностика отека несложна — это утолщение и изменение кожи, которая становится теплее или холоднее, при надавливании надолго остается ямочка.
При прогрессирующем ухудшении самочувствия и тяжести состояния у истощенного пациента отмечается быстрая и необъяснимая диетическим режимом прибавка в весе нескольких килограмм. Ткани утолщаются, по консистенции напоминая мягкое тесто.
Наиболее просто выявляется несимметричный лимфатический отек, типичный признак — отечность тыла стопы или кисти по типу подушки, когда невозможно собрать кожу в складочку. Сила тяжести приводит к застою жидкости сначала в нижних отделах, постепенно захватывая всю конечность снизу-вверх. При прогрессировании лимфатического отека конечность приобретает синюшный цвет с мраморными разводами, мягкие ткани значительно уплотняются и раздуваются, все это сопровождается нарастанием болевого синдрома и ограничением движений.
Отек конечности вследствие блокады оттока метастазами в паховой или подмышечно-надключичной лимфатической группе, нарастает очень быстро без тенденции к регрессии даже при максимально щадящем режиме и постоянном возвышенном положении. Конечность приобретает гигантский объем с мраморно-синюшной растрескивающейся кожей. Малейшее движение приводит к сильнейшей боли, купировать которую крайне сложно. Пациенты жалуются, что конечность распирает изнутри, и опасаются, что «может лопнуть». Сдавление сосудов отечными мышцами приводит к вторичному тромбозу вен, что усугубляет страдания пациента и чревато миграцией тромботических масс в легочные сосуды с угрозой смерти.
При синдроме верхней полой вены отек тканей буквально сдавливает верхние дыхательные пути и сосуды шеи. Язык и губы увеличиваются в размере, нередки точечные кровоизлияния в конъюнктиве глаза и ухудшение зрения. Беспокоит постоянная головная боль, при повороте головы возможен глубокий обморок. Состояние быстро ухудшается, присоединяется тяжелая легочно-сердечная недостаточность, возможна смерть из-за разрыва мозгового сосуда.
При раке любой отек прогрессивно ухудшает состояние за счёт декомпенсации сердечно-сосудистой и дыхательной системы, из-за застоя в легких и неадекватности газообмена в тканях развивается полиорганная недостаточность.
С отечным синдромом любой выраженности у онкологического пациента невозможно справиться только мочегонными препаратами, лечение отеков при раке требует комплексных мероприятий, в том числе с использованием специального оборудования и реанимационных техник, и обязательно мультицисциплинарной команды специалистов: онколога, кардиолога, реаниматолога, нутрициолога, нефролога. У врачей клиники большой опыт паллиативной помощи, в том числе успешной борьбы с тяжелыми отеками.
Список литературы:
- Суворова Г.Ю., Мартынов А.И. /Отёчный синдром: клиническая картина, дифференциальная диагностика, лечение // М.: ГЭОТАР-Медиа; 2009.
- Либис, Р.А., Лискова Ю.В./ Дифференциальная диагностика отечного синдрома: учебное пособие // Оренбург: Изд-во ОрГМА, 2011.
- López-Novoa J.M., Rodríguez-Peña A.B., Ortiz A. et al./Etiopathology of chronic tubular, glomerular and renovascular nephropathies: clinical implications // J. Transl. Med.; 2011, Vol. 9.
- Moore K.P., Wong F., Gines P. et al. /The management of ascites in cirrhosis: report on the consensus conference of the International Ascites Club // Hepatology; 2003, Vol. 38. № 1.
Источник
Восстановление после химиотерапии должно быть не полностью самопроизвольным, растянутым на месяцы процессом с неизвестными результатами. В любом случае через некоторое время неприятности лекарственного противоопухолевого лечения существенно уменьшатся, но восстановление пойдет быстрее и успешнее только под контролем врача, а лучше команды специалистов, отлично разбирающихся во всех аспектах реабилитации онкологических пациентов.
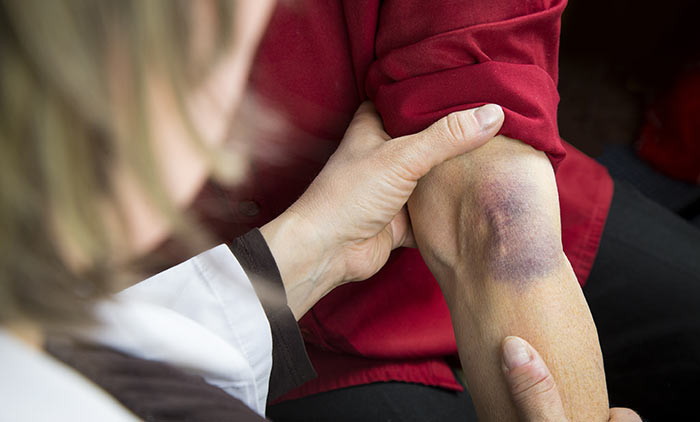
Причины появления синяков
Синяк или гематома у онкологических больных встречаются часто, потому что химиотерапия связана с внедрением в организм посредством разрушения кожных покровов — внутривенными введениями лекарств, что не всегда удается без кровоизлияния в кожу и клетчатку вокруг сосуда. Противоопухолевые лекарства изменяют состав крови, в частности численность тромбоцитов, увеличивая кровоточивость, а также впятеро повышают вероятность образования тромбов, тогда как хронически существующая варикозная болезнь увеличивает тромбообразование всего лишь вдвое.
Злокачественная опухоль меняет реологические свойства крови, приводя к образованию тромбов. У каждого пятого пациента ещё до операции выявляют скрытый тромбоз. При раке кишечника и поджелудочной железы обильное образование тромбов может быть первым признаком злокачественного заболевания. Химиотерапия, как и метастатическая стадия любой опухоли, увеличивает вероятность тромбоза в среднем в пять раз. В организме онкологического больного одновременно сосуществуют два процесса — избыточная кровоточивость и повышенная свертываемость.
Факторы риска тромбозов у онкобольных как у всех «обычных» людей: большой вес и возраст «после 40», хронические болезни сосудов и сердца, сахарный диабет, гипертония и конечно варикозная трансформация вен нижних конечностей.
К этим стандартным причинам у онкологического пациента примешиваются специфические, то есть инициируемые злокачественной опухолью и усугубляемые необходимым лечением:
- сдавливание опухолевым конгломератом кровеносных и лимфатических сосудов;
- лимфостаз после удаления подмышечных лимфоузлов, в результате облучения или удаления клетчатки малого таза с лимфоузлами, а также блок метастатическим паховыми узами оттока лимфы из ноги;
- длительный приём гормональных препаратов;
- стимуляция красного ростка кроветворения эритропоэтинами;
- постоянно установленный для частых вливаний лекарств венозный катетер;
- вынужденное из-за слабости ограничение подвижности;
- операции и облучение, а также побочные эффекты химиотерапии на сосуды и форменные элементы крови.
Для инициации тромба внутри сосуда больному раком достаточно всего трёх поводов и не обязательно сразу всех:
- повреждение внутренней оболочки сосуда, что для обычно для внутривенной химиотерапии;
- застой крови, что называют «нарушением кровообращения», в том числе в результате опухолевого конгломерата;
- избыточная свертываемость вместе с нарушением формирования сгустков.
Симптомы воспаления вен после химиотерапии
Большинство химиопрепаратов применяется только в растворе, не в таблетках, что объясняется нестойкостью лекарственных молекул к желудочному соку и сильнейшим раздражающим действием цитостатика на слизистые оболочки желудочно-кишечного тракта. При непосредственном контакте цитостатика с венозной стенкой происходит его проникновение в клетки эндотелия с изменением структуры ДНК. Произошедшая химическая реакция направляет эндотелиальную клетку к воспалительным изменениям либо к смерти — апоптозу. Повреждение усугубляется травмой стенки вены инъекционной иглой или катетером.
Воспаление венозной стенки — флебит, к которому быстро подключаются факторы риска образования тромбов, и в поврежденной химиотерапией вене развивается тромбофлебит.
Флебит проявляется болью, причём в процессе введения цитостатика боль может быть очень интенсивной, и не только в месте инъекции, но по всей руке, когда больной как будто ощущает движение лекарства по сосудистой сети, так и говорят, что «вена горит». Боль может быть краткой, а может остаться на несколько дней и даже неделю, зависит это не только от выраженности ожога эндотелия, но и личностных особенностей больного по восприятию болевых ощущений.
Боль при прохождении лекарства приводит к спастическому сокращению вены, в ответ на которое расширяются впадающие в неё мелкие венки, на внутренней поверхности руки появляется сеточка из расширенных синих сосудиков на фоне побледневшей из-за спазма артериол кожи.
Воспаленную вену можно прощупать, она как тяж плотная из-за местной отечности тканей. Когда в просвете сосуда возникнет тромб, его тоже можно будет нащупать и увидеть при УЗ- дуплексном сканировании.
Со временем воспаление пройдет, уплотнение сосуда может остаться, кожа над ним может потемнеть. Внутренний просвет сосуда после нескольких химиотерапевтических ожогов уменьшится вплоть до закрытия — облитерации. За время течения флебита откроются и расширятся подходящие к больной вене мелкие сосудики — коллатерали, но останется вероятность небольшой отечности руки ниже места венозного повреждения.
Основные методы лечения вен
После внедрения цитостатика внутрь клеток остается только ждать завершения побочного процесса и помогать восстановлению.

Патофизиология лекарственного токсического флебита мало изучена, клинических исследований по проблеме не проводилось, все рекомендации базируются только на личном опыте медицинского персонала. В каждом случае и после каждого введения необходимо консультироваться с лечащим врачом, знающим особенности локального взаимодействия цитостатика и спектр местных побочных реакций.
Для купирования болевого синдрома и уменьшения воспаления лучше всего подходят НПВС — нестероидные противовоспалительные средства, но не доказано преимуществ какого-либо одного препарата, лучше опираться на «житейские» предпочтения пациента, потому что и чувствительность к боли разная, и обезболивающий эффект тоже индивидуален.
При высоком риске легочной тромбоэмболии пациенту назначается специальная — «разжижающая кровь» терапия, как правило, длительная — никак не менее недели и при регулярном контроле свертываемости.
Можно использовать мази с гепарином для втирания в зону поврежденного сосуда. Любимый пациентами гель Гепатромбин™ состоит из гепарина и преднизолона, последний имеет противовоспалительное действие, препарат официально не сертифицирован для использования при периферическом флебите и тромбофлебите.
Хорошая репутация у мази Троксевазин™ (троксерутин), одновременно уменьшающей воспаление и отечность тканей, изменяющей реологические свойства крови в сторону разжижения, но меньше, чем это присуще гепарину. Тем не менее, исследования показали, что препарат способен растворять микротромбы.
Гель Индовазин™ представляет смесь троксерутина и НПВС индометацина, поэтому уменьшает выраженность боли и делает всё, что присуще Троксевазину™. Нецелесообразно сочетать обе мази, поскольку спектр действий комбинированного препарата больше, но с Индовазином™ вполне можно чередовать нанесение Гепатромбина™. Всасывание мазей микроскопическое, они не подменяют собой принимаемые внутрь НПВС и антикоагулянты, но помогают перенести неприятные последствия лечения.
Как восстанавливаются вены после капельниц: полезные процедуры
Местное раздражение слизистой, выстилающей внутреннюю стенку вены, пытаются уменьшить большим разведением и медленным введением в капельницах, буквально часами. Не все цитостатики выдерживают большое разведение и долгое введение, некоторые теряют свои свойства, поэтому их вводят болюсно — шприцем. В этом случае сразу же после химиопрепарата вену «моют» физиологическим раствором, стараясь уменьшить её повреждение.
Обязательно до введения и в процессе капельницы неоднократно проверяется проходимость сосуда и возможность экстравазации — распространение цитостатика в клетчатке при микроскопических разрывах сосудистой стенки.
Рекомендуется не делать химиотерапию в одну и ту же вену, лучше чередовать руки, давая сосуду больший срок на восстановление своей слизистой оболочки. Профилактическое использование мазей с гепарином или троксерутином до химиотерапии лишено патоморфологических оснований, то есть бесполезно.
При планировании многомесячной химиотерапии целесообразно подумать об установке венозного порта, срок его службы, как минимум, пятилетка. Устройство полностью исключает такой побочный эффект как лекарственный флебит, но от тромбозов спасает только приём антикоагулянтов.
Профилактика осложнений
Многие цитостатики повреждают вены, особенно усердны в инициации химических флебитов агрессивные цисплатин, антрациклины и винкаалкалоиды, а также сравнительно «мягкие» гемцитабин с фторурацилом. По действию на ткани антрациклины с винкаалкалоидами отнесены к кожно-нарывным, цисплатин всего лишь к раздражающим, а гемцитабин точно не кожно-нарывной. Тем не менее любой химиопрепарат, а тем более комбинация цитостатиков, способны повредить вену, поэтому во время внутривенного введения персонал должен строго исполнять инструкцию по длительности и способу инъекции.
Помогают восстановлению физиотерапевтические процедуры и акупунктура, фототерапия и инфракрасное облучение, стимуляция магнитным полем.
В нашей Клинике каждому больному проводится определённая и ориентированная на особенности организма и сопротивляемость тканей программа сопровождения химиотерапии и восстановления после лечения.
Список литературы:
- Российские клинические рекомендации по профилактике и лечению венозных тромбоэмболических осложнений у онкологических больных// М.: Планида; 2012
- Сомонова О.В., Антух Э.А., Елизарова А.Л., с соавтр. /Практические рекомендации по профилактике и лечению тромбоэмболических осложнений у онкологических больных // Злокачественные опухоли: Практические рекомендации RUSSCO #3s2; 2017 (том 7).
- Antithrombotic Therapy and Prevention of Thrombosis, 9th ed: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines// Chest Am Coll Chest Phys.; 2012.
- Jones S., Holmes F., O´Shaughnessey J., et al. /Docetaxel with cyclophosphamide is associated with an overall survival benefit compared with doxorubicin and cyclophosphamide: 7-year follow-up of US Oncology Re trial 9735// JCO 2009; 27.
- International Society of Lymphology. The diagnosis and treatment of peripheral lymphedema: 2013 Consensus Document of the International Society of Lymphology// Lymphology; 2013 Mar; 46(1).
- Khorana A.A., Kuderer N.M., Culakova E., et al./ Development and validation of a predictive model for chemotherapy-associated thrombosis// Blood 2008; 15.
Источник
