Ангионевротический отек конечностей фото
Ангиоотек – это патологическое состояние, сопровождающееся накоплением жидкости в тканях кожи и подкожной жировой клетчатке из-за увеличения проницаемости стенок сосудов микроциркуляторного русла. Проявляется отеком кожи различной локализации (лицо, шея, конечности), нередко сочетающимся с крапивницей и кожным зудом. Диагностика производится путем физикального осмотра, лабораторных исследований крови, изучения наследственного и аллергологического анамнеза больного. Терапевтическая тактика зависит от причин, вызвавших развитие синдрома, может включать назначение антигистаминных средств, андрогенов, ингибиторов фибринолиза и диуретиков.
Общие сведения
Ангиоотек впервые был описан в 1882 году немецким ученым Генрихом Квинке. Исследователь считал его самостоятельным заболеванием – ангионевротическим отеком. В настоящее время установлено, что примерно половина случаев патологии возникает вследствие аллергических процессов реагинового типа, тогда как остальные являются самостоятельными приобретенными или наследственными состояниями. К понятию «изолированный ангиоотек» относят целый ряд болезней, в основе которых лежат нарушения циркуляции жидкости между кровеносной системой и тканями. Ангиоотеки могут диагностироваться в любом возрасте, у женщин выявляются примерно в 1,5-2 раза чаще, нежели у мужчин. Генетически обусловленные варианты патологического состояния передаются по аутосомно-доминантному типу.
Ангиоотек
Причины ангиоотека
Существует огромное количество внешних и внутренних факторов, способствующих развитию ангионевротического отека. Непосредственной причиной патологии являются изменения в системе комплемента и нарушение некоторых других физиологических процессов (коагуляции крови, фибринолитических и кининовых реакций). В подавляющем большинстве случаев аномалия вызывается дефицитом или недостаточной активностью С1-ингибитора – протеазы крови, замедляющей и останавливающей ряд биохимических реакций в крови и тканях. Данное явление возникает под влиянием следующих факторов:
- Генетические особенности. Значительная часть эпизодов врожденного ангиоотека обусловлена мутацией гена SEPRING1, расположенного на 11-й хромосоме. Он кодирует белковую последовательность С1-ингибитора, поэтому при изменении данного гена отмечается дефицит протеазы или потеря ее функции.
- Лимфопролиферативные патологии. Некоторые состояния с ускоренным размножением лимфоцитов или их клеток-предшественников (например, лимфомы) могут сопровождаться ангионевротическими отеками. Причина этого кроется в увеличении скорости разрушения С1-ингибитора.
- Аутоиммунные реакции. При определенных условиях формируются антитела к C1-эстеразе, связывающие этот фермент и способствующие его разрушению. Процесс может возникать как изолированно, так и при системных аллергических реакциях или иных нарушениях.
Редким вариантом патологии является ангиоотек, развивающийся при оптимальном уровне С1-ингибитора – в основном к нему относят так называемые эстрогензависимые отеки. Предполагают, что они обусловлены генетическими факторами и передаются по сцепленному с Х-хромосомой механизму, течение заболевания усугубляется при приеме препаратов эстрогена. Также существует разновидность болезни, провоцируемая использованием ингибиторов ангиотензин-превращающего фермента, входящих в состав многочисленных антигипертензивных средств.
Патогенез
Возникающий по той или иной причине дефицит С1-ингибитора приводит к активации системы комплемента, увеличивает концентрацию калликреина и брадикинина. Последние стимулируют образование вазоактивных пептидных соединений, воздействующих на сосудистые стенки и гладкую мускулатуру. В результате происходит сначала расширение прекапиллярных артериол, затем – выход элементов плазмы клетки из кровеносного русла в межклеточное пространство. Таким образом, формируется локальный ангиоотек, проявляющийся характерной клинической картиной. Кроме того, реакции брадикининового звена могут вызывать спазм гладкомышечных клеток пищеварительной и дыхательной систем, нарушая их моторику.
Классификация
С учетом особенностей клинического течения в клинической аллергологии все случаи ангиоотека делят на две большие группы – изолированные и сочетанные. Первые проявляются только отеком подкожной жировой клетчатки и кожи, вторые могут сопровождаться крапивницей, спазмом дыхательных путей и другими симптомами. Разделение является достаточно условным, слабо отражает причины заболевания. По этиологическому признаку выделяют наследственные и приобретенные формы ангионевротического отека. Врожденные разновидности составляют примерно 2-5% от общего количества случаев болезни, включают следующие типы:
- Тип 1. Обусловлен почти полным отсутствием С1-ингибитора, возникающем при мутации гена SEPRING1. Характеризуется довольно тяжелым течением – генерализованностью и выраженностью отеков, их появлением не только на коже, но и на слизистых дыхательных путей или пищеварительного тракта. Регистрируется в 85% случаев наследственного ангиоотека.
- Тип 2. Развивается при относительном недостатке ингибитора вследствие его медленного образования или пониженной активности из-за неправильной структуры фермента. Клиника менее тяжелая, отеки поражают преимущественно ткани конечностей, иногда лица. Такой вариант заболевания диагностируется у 12-14% больных с наследственными формами ангионевротического отека.
- Тип 3. Встречается крайне редко, обычно – на фоне отсутствия дефицита С1-эстеразы. Как правило, представлен эстрогензависимыми отеками – обострениями патологии при беременности, приеме комбинированных оральных контрацептивов, заместительной терапии в период климакса.
Все варианты наследственного ангиоотека являются изолированными, не сопровождаются крапивницей или иными нарушениями. Приобретенные разновидности имеют другую классификацию, включающую в себя всего два основных типа заболевания:
- Тип 1. Выявляется на фоне лимфопролиферативных состояний – лимфом, при некоторых инфекционных поражениях. Причиной становится увеличение потребления С1-ингибитора и его последующий недостаток.
- Тип 2. Возникает из-за синтеза аутоантител к ингибитору, что резко снижает его концентрацию в крови. Такое явление имеет место при некоторых аутоиммунных и аллергических состояниях, иммунодефицитах и других патологиях.
Симптомы ангиоотека
Основным симптомом патологии является появление безболезненного отека кожи различного размера. Больные отмечают ощущение распирания и напряжения, иные субъективные жалобы отсутствуют. В отличие от воспалительных отеков пораженная область характеризуется более бледным, нежели окружающие участки кожи, цветом и отсутствием локального повышения температуры тканей. Чаще всего отечные проявления обнаруживаются на верхних и нижних конечностях, лице (губы, щеки, веки, ушные раковины), шее, в зоне половых органов. Кожный зуд нехарактерен, но может определяться при сочетании ангиоотека с крапивницей.
У некоторых больных отек выявляется в области слизистых оболочек, иногда патологический процесс затрагивает и подслизистую пластинку. Наиболее часто поражаются органы полости рта (язык, мягкое небо), дыхательные пути, желудочно-кишечный тракт. При развитии ангиоотека органов респираторной системы возникает ощущение нехватки воздуха, осиплость или полная потеря голоса, лающий кашель. Вовлечение ЖКТ проявляется выраженным абдоминальным синдромом – болями, тошнотой, рвотой. Отмечается напряжение мышц брюшной стенки, создающее ложную картину перитонита или острой кишечной непроходимости.
Крайне редкими симптомами заболевания являются признаки плеврального выпота (кашель, боль в груди, затрудненное дыхание). В число других редких вариантов патологии входит локальный отек головного мозга (регистрируется угнетение сознания, гемипарезы), ангиоотек мочевого пузыря (сопровождается острой задержкой мочи), поражение мышц и суставов. Изолированные формы заболевания развиваются медленно на протяжении 12-48 часов. После этого при отсутствии осложнений происходит медленное разрешение отечности в течение 5-8 дней. Некоторые сочетанные варианты ангионевротического отека (особенно аллергического генеза) могут прогрессировать намного быстрее – в течение нескольких минут или часов.
Осложнения
Вероятность осложнений при ангиоотеке зависит от локализации патологического процесса. Наиболее часто (примерно в половине от всех осложненных случаев) у больных возникают затруднения дыхания, обусловленные сужением просвета гортани или бронхов. При отсутствии медицинской помощи нарушение может стать причиной летального исхода. Относительно опасны абдоминальные формы патологии, которые могут вызывать расстройства перистальтики с развитием непроходимости и перитонита. Нередко отеки органов ЖКТ становятся причиной ненужного хирургического вмешательства из-за ошибочной диагностики. Поражение головного мозга способно привести к коме и ряду неврологических последствий (нарушения координации, речи, восприятия). Острая задержка мочи при отечных явлениях в мочевом пузыре является причиной рефлюкса жидкости, гидронефроза и почечной недостаточности.
Диагностика
В большинстве случаев диагноз ангионевротический отек выставляет врач-иммунолог. Реже с этой патологией сталкиваются специалисты иных направлений – дерматологи, педиатры, гастроэнтерологи, терапевты. Определение заболевания часто затруднено из-за его разнообразной этиологии и очень широкого спектра клинических проявлений. Основное внимание уделяют анамнестической информации и результатам специфических лабораторных исследований. Диагностика ангиоотека включает в себя следующие методики:
- Опрос и осмотр. При наружном осмотре уточняют распространенность и локализацию отечного участка, подтверждают отсутствие болезненности. Методом расспроса выясняют, что предшествовало развитию патологических проявлений (стресс, употребление каких-либо продуктов, прием лекарств), имели ли место подобные реакции у родственников.
- Лабораторные анализы. Специфическим методом диагностики ангиоотека является определение уровня С1-ингибитора плазмы крови – его отсутствие или снижение количества свидетельствует в пользу наличия заболевания. Возможно определение титра антител к С1-ингибитору – эта методика позволяет выяснить, имеет ли болезнь приобретенный аутоиммунный характер.
- Дополнительные исследования. При поражении дыхательной системы производят бронхоскопию, рентгенографию органов грудной клетки. Обычно выявляется отек тканей гортани, бронхоспазм, изредка обнаруживается плевральный выпот. УЗИ органов брюшной полости позволяет дифференцировать абдоминальные формы ангиоотека от перитонита и других патологий органов ЖКТ.
Помимо вышеперечисленных методов при диагностике данного состояния учитывают огромное количество разнообразных факторов. Например, возраст больного: наследственные разновидности чаще обнаруживаются у лиц младше 20 лет, приобретенные формы – у людей старше 40 лет с отягощенным анамнезом. Принимают во внимание наличие или отсутствие сопутствующих симптомов – крапивницы, дыхательных расстройств. Дифференциальную диагностику проводят с отеками иного генеза – в результате почечной патологии, укуса ядовитых насекомых, локальных аллергических и воспалительных реакций.
Лечение ангиоотека
Терапевтические мероприятия при ангионевротическом отеке разделяют на две группы – методы для купирования острого приступа и техники для профилактики его последующего развития. В обоих случаях используют сходные лекарственные вещества – в зависимости от целей их назначения меняется только схема приема и дозировка. Наиболее часто для лечения ангиоотека в современной иммунологии применяют следующие препараты:
- Андрогены. Некоторые аналоги мужских половых гормонов (даназол, метилтестостерон) способны усиливать синтез С1-эстеразы в клетках печени. Они уменьшают выраженность симптомов патологии и снижают вероятность приступа заболевания в будущем.
- Ингибиторы фибринолиза. Лекарственные средства, препятствующие фибринолитическим процессам, также замедляют реакции калликреинового пути. Благодаря этому снижается скорость диффузии плазмы в ткани, уменьшается вероятность возникновения ангиоотека. Применение препаратов данной группы (е-аминокапроновая или транексамовая кислоты) проводят под контролем состояния свертывающей системы крови.
- Свежезамороженная плазма. Переливание донорской плазмы, содержащей в себе С1-ингибитор, является эффективным методом купирования острых отеков, особенно наследственного характера.
При наличии аутоантител против компонентов комплемента показано их удаление из кровотока с помощью плазмафереза. Это временная мера, способная значительно ослабить выраженность отечных проявлений. При угрозе жизни больного (например, из-за обтурации дыхательных путей) рекомендуется введение адреналина, а при его неэффективности – конико- или трахеотомия. Если причиной ангиоотека послужило наличие другого заболевания (аллергического, аутоиммунного или иного характера) – разрабатывается схема его лечения согласно показаниям. Существуют также перспективные препараты ингибитора, использующиеся в некоторых странах для терапии данного состояния.
Прогноз и профилактика
Прогноз ангиоотека считается неопределенным до выяснения его этиологии у конкретного больного. При наследственном характере патологии всегда существует риск развития летального отека гортани, поэтому пациентам желательно иметь при себе карточку с указанием диагноза. При правильном профилактическом лечении приступы возникают редко, не представляют угрозы для жизни больного. Прогноз приобретенных форм зависит от характера основного заболевания. Профилактические мероприятия включают в себя своевременное лечение аллергических и аутоиммунных состояний.
Источник
Недостаток ингибитора С1-эстеразы (С1-INH) – редкая патология иммунной системы, вызывающая спонтанные приступы ангионевротического отека из-за избытка брадикинина. Они доставляют пациенту большой дискомфорт, приводят к психоэмоциональным расстройствам, ухудшают качество жизни и могут быть опасными для жизни. Ангионевротический отек, вызванный брадикинином, – редкое заболевание, обычно наследуемое по аутосомно-доминантному типу.
Ангионевротический отек – распространенный симптом в клинической практике, с которым может столкнуться любой врач. Следовательно, очень важно уметь распознавать и дифференцировать происхождение этого клинического симптома.
Что такое ангионевротический отек
Ангионевротический отек – это внезапный отек более глубоких слоев кожи и подкожной клетчатки. Этот симптом при крапивнице может сочетаться с высыпанием волдырей. В этом случае ангионевротический отек вызван высвобождением гистамина. Отек Квинке также может развиваться при количественной или качественной дисфункции компонентов комплемента. В этом случае ангионевротический отек диагностируется как отдельное заболевание.
![]() Крапивница
Крапивница
Белок, регулирующий комплемент, C1-INH – это фермент, который регулирует количество брадикинина в организме. Недостаток этого фермента вызывает ангионевротический отек, поскольку он нарушает регуляцию систем калихреина и хинина и приводит к выработке значительно большего количества брадикинина.
Дефицит C1-INH может быть как врожденным, так и приобретенным. Наследственный ангионевротический отек, вызванный дефицитом C1-INH, встречается у 1 из 50000 человек. У людей приобретенный ангионевротический отек, вызванный дефицитом C1-INH, встречается еще реже – 1 на 600 тыс. людей в мире.
Цель статьи – обзор патогенеза, диагностики, дифференциальной диагностики и принципов лечения ангионевротического отека с дефицитом C1-INH.
Клиническое проявление и дифференциальный диагноз
В научной литературе ангионевротический отек может быть обозначен как отек Квинке, ангионевротический отек, гигантская крапивница. При ангионевротическом отеке изменения происходят в глубоких слоях кожи и под кожей. Клинически это проявляется в виде асимметричного отека и припухлости определенного участка тела.
Одним из распространенных сопутствующих и раздражающих пациентов симптомов является боль. Кожа в месте инъекции может оставаться неизменной или может возникнуть покраснение размытых линий. Отек сохраняется до 72 часов или даже дольше.
Ангионевротический отек может возникнуть на любом участке тела – губах, языке, лице, конечностях и т.д. При каждом приступе ангионевротического отека опухоль и припухлость могут быть на разных участках.
- Ангионевротический отек лица вызывает дискомфорт и нарушает повседневную деятельность.
- Ангионевротический отек гортани – острое и опасное для жизни состояние. При отсутствии лечения ангионевротический отек гортани приводит к смерти примерно в 25-40% случаев. У любого пациента с дефицитом C1-INH приступ ангионевротического отека гортани может возникнуть хотя бы один раз в жизни.
- Отек Квинке также может возникать во внутренних органах, таких как стенка кишечника. Это вызывает боли в животе, тошноту, рвоту, диарею, общую слабость – все эти симптомы относят к острому абдоминальному синдрому, наиболее частой причиной которого является аппендицит.
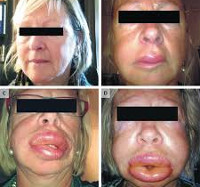
![]() Отек Квинке
Отек Квинке
Своевременное распознавание ангионевротического отека из-за дефицита C1-INH может обеспечить соответствующее лечение и избежать ненужного хирургического вмешательства. Это важно, так как клинические исследования показали, что пациенты с дефицитом C1-INH часто подвергались ненужным хирургическим вмешательствам. При соответствующем лечении можно предотвратить или снизить частоту спонтанного ангионевротического отека.
Ангионевротический отек диагностируется на основании истории болезни пациента и объективного обследования. Патологию следует дифференцировать от:
- Анасарка – это широко распространенный отек мягких тканей, которое является симметричным и является клиническим признаком других заболеваний, таких как недостаточность почек, микседема;
- Псевдоангионевротического отека, например, при синдроме компрессии верхней полой вены;
- Синдрома Мелкерссона-Розенталя – нейропатии, которая клинически может проявляться отеком лица или губ).
Ангионевротический отек из-за дефицита C1-INH встречается гораздо реже и устойчив к лечению антигистаминными препаратами, системными глюкокортикоидами и адреналином.
Если подозревается ангионевротический отек из-за дефицита C1-INH, рекомендуется тест на компонент комплемента 4 (C4). C4 снижается даже при ремиссии и всего на 5% у всех пациентов остается неизменным или повышенным.
Диагноз подтверждается исследованием активности (функции) и количества C1-INH. Также проводится тестирование на антитела к C1-INH. При наследственном ангионевротическом отеке титр антител C1-INH в норме, а при приобретенном ангионевротическом отеке снижается у 70% пациентов.
Роль C1-INH и патогенез ангионевротического отека из-за дефицита
C1-INH C1-INH непосредственно участвует в системе калькреина и кинина, а также в регуляции медиатора воспаления брадикинина. Недостаток этого фермента приводит к нарушению метаболических путей калихреина и кинина и чрезмерной продукции брадикинина.
Ангионевротический отек из-за дефицита C1-INH делится на четыре типа, основные отличия которых представлены в таблице 1. C1-INH является представителем семейства серпинов, ингибитором сериновой протеазы. Ген C1-INH находится на хромосоме 11 и называется SERPING1. Именно мутации в этом гене вызывают дефицит C1-INH.
Если мутация в этом гене обнаружена, ангионевротический отек классифицируется как первый тип, т.е. ангионевротический отек, наследуемый по аутосомно-доминантному типу. Около 75%. пациентов с этой мутацией указывают на то, что случаи этого заболевания находятся в семье, но около 25%. Мутация de novo выявляется во всех случаях заболевания.
При третьем типе ангионевротического отека эндогенный C1-INH ингибирует протеазы и факторы (например, XII и XIIa), участвующие в физиологических каскадах систем комплемента, калькреина и кинина. Эти системы участвуют в таких процессах, как коагуляция и фибринолиз.
Фактор XII автоматически активируется с образованием фактора XIIa, который расщепляет прекаликреин, который, в свою очередь, генерирует плазменный калькреин. Каликреин в плазме активирует фактор XII, который регенерирует фактор XIIa и расщепляет макромолекулярный кининоген, высвобождающий брадикинин.
Медиатор воспаления брадикинин связывается с рецепторами В2, которые находятся на поверхности клетки, и образуют комплекс. Этот комплекс вызывает расширение сосудов, увеличивает проницаемость эндотелия сосудов. Весь каскад этих процессов вызывает ангионевротический отек.
Снижение уровня C1-INH выявляется не во всех случаях. Количество этого фермента может быть достаточным, но функция может быть нарушена. Такой патогенез характерен как для врожденного, так и для приобретенного ангионевротического отека.
Таблица 1. Типы ангионевротического отека из-за дефицита C1-INH
| Первый тип | Второй тип | Третий тип | Четвертый тип |
| Врожденный | Врожденный | Врожденный | Приобретенный |
| C1-INH – это C4 ↓, C1q – норма | Уровни C1-INH и C4, C1q являются нормой | Уровни C1-INH и C4, C1q являются нормой | Количество C1-INH и C4, C1q ↓ |
| Функция C1-INH не нарушена | Функция C1-INH нарушена или нормальна | Функция C1-INH не нарушена | Функция C1-INH нарушена |
| Мужчины и женщины – 1: 1 | Мужчины и женщины – 1: 1 | Мужчины < женщины | Мужчины и женщины – 1: 1 |
| 85 процентов. во всех случаях дефицита C1-INH | 15 процентов во всех случаях дефицита C1-INH | Наименее распространенный тип | Очень редко |
| Пациенты младше 20 лет | Пациенты младше 20 лет | Больные женщины старше 40 лет | Больные люди более 40 лет пациентов |
| Мутация на хромосоме 11 (SERPING1) *. Унаследовано по аутосомно-доминантному типу. 75%. семейный анамнез (+) , 25% – мутация de novo | Точечная мутация | Мутации в генах ANGPT1 * или PLG * | Может спровоцировать сопутствующие заболевания гематологического или аутоиммунного происхождения. Нет семейной истории |
* SERPING1 – англ. Ингибитор серпин-пептидазы Clade G Member 1, ANGPT1 – ангиопротеин 1, PLG – плазминоген.
Принципы лечения отека Квинке, вызванного дефицитом C1-INH
Чтобы избежать приступов отека Квинке, рекомендуется избегать провокационного фактора, который может включать стресс, травму или оральные контрацептивы. Однако часто основная причина отека Квинке неизвестна, и он возникает спонтанно.
Ангионевротический отек из-за дефицита C1-INH не связан с крапивницей или другими аллергическими заболеваниями, при которых гистамин является одним из основных факторов патогенеза. Следовательно, лечение ангионевротического отека, вызванного брадикинином, антигистаминными препаратами, глюкокортикоидами и / или адреналином неэффективно.
Для лечения ангионевротического отека из-за дефицита C1-INH может быть назначено симптоматическое или профилактическое лечение. Симптоматическое лечение – это прием лекарства во время приступа ангионевротического отека.
![]() Симптоматическое лечение ангионевротического отека
Симптоматическое лечение ангионевротического отека
Основные препараты, применяемые при приступах приобретенного и врожденного острого ангионевротического отека, – концентрат C1-IHN, антагонист рецептора B2 икатибант и ингибитор каликреина экалантид. Если эти препараты недоступны, возможно лечение плазмой, обработанной растворителем-детергентом (SDP) или свежезамороженной плазмой.
Профилактическое лечение – это прием медикаментов для предотвращения приступа отека Квинке. Оно может быть краткосрочным или долгосрочным.
- Цель длительного профилактического лечения – снизить частоту и тяжесть спонтанных приступов ангионевротического отека. Длительное профилактическое лечение считается эффективным, когда частота возникновения ангионевротического отека снижается более чем на 50%.
- Цель краткосрочного профилактического лечения – предотвратить ангионевротический отек во время запланированной процедуры или вмешательства, например, вмешательства стоматологического происхождения.
Лекарства для лечения отека Квинке, вызванного дефицитом C1-INH
Для симптоматического и профилактического лечения используется производное C1-INH в плазме крови, которое увеличивает концентрацию C1-INH в плазме. Синтетический концентрат C1-INH человека используется для лечения ангионевротического отека с 1970-х годов. В настоящее время также вводятся синтетические концентраты C1-INH. Исследования показали, что использование производного плазмы C1-INH в дозе 1000 МЕ 2 м.т. в неделю снижает частоту спонтанных приступов ангионевротического отека на 50% по сравнению с плацебо.
Синтетические андрогены – даназол и станозол – используются как в краткосрочной, так и в долгосрочной профилактике. Результаты двойного слепого плацебо-контролируемого исследования показали, что андрогены снижают тяжесть и частоту ангионевротического отека. Правда, такое лечение связано с риском побочных эффектов. Наиболее частые побочные эффекты, вызываемые андрогенами, – увеличение волос, вес, артериальное давление, активность ферментов печени и изменение голоса.
![]() Синтетический андроген – даназол
Синтетический андроген – даназол
Angioedem также лечится экалантидом. Это рекомбинантный белок из 60 аминокислот, прямой ингибитор каликреина. Исследования показали, что он сокращает продолжительность отека Квинке примерно на 5%. У всех испытуемых наблюдались аллергические реакции. Эккалантид лучше всего подходит для лечения острого ангионевротического отека.
Еще одно лекарство, используемое для лечения ангионевротического отека, – это икатибант, антагонист рецептора B2. Хорошо переносится. По данным недавних клинических испытаний, икатибант составляет примерно 80%. Нежелательные явления наблюдались не у всех пациентов. Икатибант показал свою эффективность при лечении ангионевротического отека 1 и 2 типа и ангионевротического отека, вызванного АПФ.
Последнее эффективное лечение – это биологическая терапия ланаделумабом. Это моноклональные антитела, которые связываются с активным калькреином в плазме. В клинических испытаниях ланаделумаб был эффективен для длительного профилактического лечения и вызывал несколько побочных эффектов. При лечении наследственного ангионевротического отека этот препарат оказался более эффективным, чем плацебо.
Лечение ангионевротического отека, вызванного дефицитом C1-INH, кратко изложено в таблице 2.
Таблица 2. Лечение отека Квинке, вызванного дефицитом C1-INH
| Острое состояние – во время приступа отека Квинке | Краткосрочная профилактика | Долгосрочная профилактика |
| Избегайте провокационных факторов: стресса, напряжения, пероральных контрацептивов и т.д. | ||
| Внутривенное вливание производного плазмы C1-INH (человеческого или рекомбинантного) | Цель – предотвратить ангионевротический отек во время запланированной процедуры или вмешательства | Цель – снизить частоту и тяжесть приступов спонтанного ангионевротического отека |
| Икатибант подкожная инъекция (антагонист рецептора брадикинина B2) | Инфузия производного плазмы C1-INH | Инфузия производного плазмы C1-INH |
| Подкожная инъекция эскалантида (ингибитор плазменного каликреина, предотвращающий превращение кининогена в брадикинин) | Препараты тестостерона: данозол, станозол | Препараты тестостерона: данозол, станозол |
| Интубация, трахеостомия | Икатибант | Икатибант |
Резюме
Ангионевротический отек из-за дефицита C1-INH – редкая патология. Он может быть как врожденным, так и приобретенным. Ангионевротический отек может возникнуть в любом месте тела. Отек гортани – распространенное и опасное для жизни состояние.
Ангионевротический отек из-за дефицита C1-INH диагностируется при выявлении дефицита или дисфункции компонента этой системы комплемента. Препарат выбора для лечения – концентрат C1-INH. Его можно использовать во время острого приступа отека Квинке или для долгосрочной и краткосрочной профилактики.
Источники: Ридл М.А., Гривчева-Пановская В., Молдован Д. и др. Рекомбинантный ингибитор С1-эстеразы человека для профилактики наследственного ангионевротического отека: многоцентровое рандомизированное двойное слепое плацебо-контролируемое перекрестное исследование фазы 2. Ланцет, 2017; Буссе П.Дж., Смит Т. Гистаминергический ангионевротический отек. Клиники иммунологии и аллергии Северной Америки, 2017; Ловерде Д., Files DC, Кришнасвами Г. Ангионевротический отек. Реанимационная медицина, 2017; Radonjic-Hoesli S, Hofmeier KS, Micaletto S, et al. Крапивница и ангионевротический отек: обновленная информация о классификации и патогенезе. Клинические обзоры в аллергии и иммунологии, 2017; Зеерледер С., Леви М. Наследственный и приобретенный C1-ингибитор-зависимый ангионевротический отек: от патофизиологии к лечению. 2016; Заничелли А., Азин Г.М., Ву М.А. и др. Диагностика, течение и лечение отека Квинке у пациентов с приобретенным дефицитом ингибитора C1. Журнал аллергии и клинической иммунологии: на практике, 2017; Буссе П.Дж. и др. Ланаделумаб для профилактического лечения наследственного ангионевротического отека с дефицитом ингибитора С1: обзор доклинических исследований и исследований фазы I. BioDrugs, 2018; Хориучи Т. Наследственный ангионевротический отек с 1888 по 2018 год – прогресс и проблемы. Демпстер Дж. (2018). Практические аспекты применения концентрата C1-INH в уменьшенном объеме для лечения наследственного ангионевротического отека: практический опыт. Аллергия, астма и клиническая иммунология, 2018; Фирст Р., Даффи Х. (2015). Лечение острых приступов наследственного ангионевротического отека: роль экалантида. Journal of Blood Medicine, 2015; Banerji A, et al. Эффект ланаделумаба по сравнению с плацебо на профилактику наследственных приступов ангионевротического отека. JAMA, 2108. Медицина внутренних органов, 2019; Cicardi M, et al. HAWK под патронатом EAACI. Классификация, диагностика и подход к лечению ангионевротического отека: консенсусный отчет Международной рабочей группы по наследственному ангионевротическому отеку. Аллергия, 2014; Отани И.М., Банерджи А. Приобретенный дефицит ингибитора С1. Клиники иммунологии и аллергии Северной Америки, 2017; Lewis LM, et al. Экаллантид для неотложного лечения ангионевротического отека, индуцированного ингибитором ангиотензинпревращающего фермента: многоцентровое рандомизированное контролируемое исследование. Анналы неотложной медицины, 2015; Валериева А. и др. Рекомбинантный ингибитор C1-эстеразы человека (Cone alfa) для профилактики приступов у взрослых и подростков с наследственным ангионевротическим отеком. Обзор клинической иммунологии, 2018.
Источник
