Протокол лечения отека головного мозга

ГЛАВА 19 ОТЕК МОЗГА
19.1. ОБЩИЕ ПОЛОЖЕНИЯ
Отек
головного мозга (oedema cerebri) – патологический процесс,
характеризующийся накоплением воды в головном мозге, увеличением его
массы и объема. Вода может накапливаться как в межклеточных
пространствах, так и внутри клеток. Нередко отек мозга сначала имеет
ограниченный характер, а в последующем распространяется на все более
обширные территории мозга. Обычно отек ведет к повышению
внутричерепного давления.
Патофизиологическим
фактором, способствующим развитию отека мозга, является гипоксия. Она
влечет за собой своеобразный каскад патофизиологических явлений:
увеличение парциального давления углекислого газа в крови (РаСО2)
=> тканевый ацидоз => начинающийся отек мозговой ткани =>
замедление артериального кровотока => нарушение ликвороциркуляции
=> затруднение венозного оттока из полости черепа => нарастание
выраженности отека мозга, при этом, как правило, возникает
дезорганизация функций гематоэнцефалического барьера (ГЭБ), изменение
мембранного потенциала клеток мозга, нарушение транспорта ионов через
клеточные мембраны, их патологическое накопление и избыточное
количество жидкости во внеклеточных и внутриклеточных пространствах.
Раньше
внутриклеточное накопление воды признавалось набуханием, отеком же
считалось лишь увеличение количества воды в межклеточных пространствах.
Однако эти процессы проходят обычно параллельно и их дифференциация в
связи с этим не оправдывается. Потому все процессы накопления воды в
мозге стали именоваться его отеком, хотя некоторые авторы предпочитают
говорить об отеке-набухании. Также существует мнение, что термином
«набухание мозга» следует обозначать гиперемию мозговой ткани (Потапов
А.А., Гайтур Э.И., 1998), возникающую, в частности, при его
травматическом по- ражении.
19.2. ВАРИАНТЫ ОТЕКА МОЗГА
Отек головного мозга всегда ведет к увеличению его объема и массы и, как следствие, к повышению внутричерепного давления. Значима
не только распространенность отека, но и его локализация. Повышенную
опасность для больного имеет отек медиобазальных отделов височной доли,
часто приводящий к вклинению ее ткани в вырезку намета мозжечка (в
тенториальное отверстие),
отек мозжечка, рано вызывающий блокаду ликворных путей и развитие окклюзионной гидроцефалии, а также отек ствола мозга.
Возможны различные причины отека мозга: травма
мозга, нарушение мозгово- го кровообращения, в частности
гипертонический криз, острая гипертоническая энцефалопатия,
геморрагический инсульт, инфаркты, а также опухоли мозга, эн- цефалиты
или менингоэнцефалиты, гипоксическая или токсическая (эндогенная или
экзогенная) энцефалопатия, облучение мозга, эпилептический статус.
В
патогенезе отека мозга преобладающими могут быть сосудистые
(вазогенные), тканевые (интерстициальные) факторы, цитотоксические
(дисметаболические) и осмотические процессы. Они отличаются друг от
друга особенностями биохимических и патофизиологических механизмов
развития и распределения в мозговой ткани отечной жидкости. Преобладание
проявлений той или иной формы отека мозга зависит от многих
обстоятельств, в частности от характера обусловившего его
патологического процесса и возраста больного.
В основе вазогенного отека лежит
значительное повышение давления в капиллярах мозга, расширение в них
межэндотелиальных щелей, при этом увеличивается перфузионное давление в
сосудах мозговой ткани, повышается проницаемость ГЭБ, происходит выход
коллоидных компонентов плазмы во внеклеточную жидкость, что
способствует усилению фильтрации в межклеточные пространства мозга
воды, которая в значительном количестве скапливается в белом веществе. Вазогенный отек развивается при острых нарушениях мозгового кровообращения, энцефалите, незрелой глиальной опухоли.
Интерстициальный отек мозга является
также формой межклеточного отека, обусловленного прежде всего
нарушением ликвороциркуляции, особенно выраженным при окклюзионной
гидроцефалии. Жидкость проникает через выстилающий желудочки
мозга слой эпендимных клеток (эпендимоциты) в паравентрикулярно
расположенные структуры белого вещества мозга.
Цитотоксический (дисметаболический) отек мозга обусловлен повреждающими мозг экзогенными и эндогенными факторами и нарушением в нем метаболических процессов, проявляется
расстройством функции энергозависимых мембранных натрий-калиевых
ионных насосов и деполяризацией клеточных мембран, наступающей при
снижении уровня мозгового кровотока. Деполяризация мембран ведет к
электролитному дисбалансу, повышению осмотического давления в
клеточных элементах мозговой ткани и накоплению в них жидкости.
Осмотический отек развивается в
результате патологичных изменений осмотического градиента между
плазмой крови и жидкости в межклеточных про- странствах мозговой ткани,
особенно выражен при остром поражении мозга у детей,
развивается также при чрезмерно ускоренном гемодиализе у больных с
уремией на фоне острой или хронической почечной недостаточности и прояв- ляется как в белом, так и сером веществе мозга. В
эксперименте на обезьянах доказано, что при осмотическом отеке в мозге
изменяется количество таких ферментов, как лактатдегидрогеназа,
креатинфосфокиназа, усиливается анаэ- робный гликолиз, возрастает
количество молочной кислоты.
По распространенности различают локальный, трифокальный, долевой полушарный и диффузный отек мозга. Возникающая
при отеке мозга клиническая картина обусловлена дисфункцией
подвергшейся отеку мозговой ткани, расстройством в ней микроциркуляции,
метаболических процессов и возникающим при этом увеличением объема
мозговой ткани, которое может сопровождаться смещением, а иногда и
вклинением определенных мозговых структур, нарушениями кровотока в
сосудах мозга и ликвородинамики.
При выраженном
отеке мозга обычно возникает сочетание всех проявлений, характерных для
отмеченных вариантов. В отечной ткани оказывается выраженным снижение
артериовенозной разницы по кислороду, снижается потребление кислорода
клеточными структурами, нарастает накопление продуктов нарушенного метаболизма.
Для клинической картины выраженного отека мозга характерны общемозговые симптомы (снижение уровня психической активности, загруженность, диффузная головная боль), которые могут сочетаться с появлением или нарастанием очаговых неврологических симптомов, выраженность которых резко увеличивается в случаях смещения и вклинения отечных мозговых структур.
На
КТ и МРТ отечная ткань мозга характеризуется пониженной плотностью. По
результатам повторных КТ- и МРТ-исследований можно следить за
изменениями объема мозговой ткани и выявляемой в ней зоны отека, за
сопутствующими деформациями мозговых структур и изменением формы и
размера желудочков мозга и таким образом контролировать в динамике
выраженность отека. На основании КТ- и МРТ-исследований установлено,
что при распространении отека на глубинные структуры мозга вектор
клиренса отечной жидкости направлен в сторону ближайшей стенки
желудочковой системы мозга. Об этом свидетельствует нередкое выявление
на КТ гиподенсивной дорожки от зоны перифокального отека к прилежащим
отделам желудочковой системы.
При
макроскопическом осмотре отечного мозга обращает на себя внимание
увеличение его объема и влажности, на разрезе – нечеткость границ между
серым и белым веществом. Гистологическое исследование позволяет
выявить расширение межклеточных и околососудистых щелей, изменения
эндотелия капилляров, увеличение объема нейронов и особенно глиальных
клеток (астроцитов и олигодендроцитов), утолщение нервных волокон,
нарушение струк- туры миелиновой оболочки.
19.3. ЛЕЧЕНИЕ
При
появлении признаков отека мозга необходимо выявление его причины, что
может быть достигнуто уточнением клинического диагноза. Желательно, конечно, чтобы причина отека мозга была устранена, что иногда можно достичь проведением соответствующего этиологического и патогенетического консервативного лечения, например при гипертоническом кризе, контузии головного мозга, энцефалите, или хирургического вмешательства: удаление
гематомы, абсцесса, опухоли, а при черепно-мозговой травме – отломков
кости, инородных тел, подоболочечной или эпидуральной гематомы.
Во
всех случаях отека мозга, сопровождающегося внутричерепной
гипертензией, показано медикаментозное лечение, направленное на
дегидратацию мозговой ткани. С этой целью применяются осмотические
диуретики, салуретики и кортикостероиды. Различные в
каждом конкретном случае патогенетические особенности, темп развития
отека мозга и степень его выраженности не позво- ляют рекомендовать
жестких стандартных схем применения препаратов, ока- зывающих
противоотечное действие.
Показаниями к назначению осмотических диуретиков являются признаки выраженного отека мозга, остро возникающее или прогрессирующее повы-
шение
внутричерепного давления, сопровождающееся нарастающей общемозговой и
очаговой неврологической симптоматикой, смещением мозговых структур,
угрозой вклинения мозговой ткани, а также подготовка к экстренной
нейрохирургической операции.
Из осмотических диуретиков чаще применяется маннитол (15%
раствор внутривенно капельно в течение 10-20 мин из расчета 0,5-1,5
г/кг массы тела больного, повторяя введение препарата в той же дозе
через каждые 6 ч) или глицерол (0,5-1,0 г/кг внутрь,
можно в смеси с сиропом, при необходимости – через назогастральный
зонд). В процессе лечения осмолярность крови должна поддерживаться на
уровне не выше 300-310 мосм/л. Действие маннитола проявляется через 10-20 мин и продолжается 4-6 ч. Вводят маннитол или содержащий его комбинированный препарат реоглюман (внутривенно
капельно сначала по 5-10 капель, а затем 30 капель в 1 мин);
рекомендуется сделать перерыв через 2-3 мин и при отсутствии побочных
явлений продолжать введение препарата со скоростью до 40 капель/мин,
при этом вводится 200-400 мл). Эти препараты дают выраженный
дегидрирующий эффект, понижают агрегацию форменных элементов крови,
уменьшают вязкость крови и способствуют восстановлению кровотока в
капиллярах, увеличению оксигенации ткани. Суточная доза маннитола не должна превышать 140-180 г.
Надо иметь в виду проявляющиеся при введении маннитола и других осмотических диуретиков нежелательные побочные явления: 1)
вследствие увеличения при введении осмотических диуретиков объема
циркулирующей в сосудах крови возможны нарастание сердечной
недостаточности и отек легких; 2) дегидратация, обусловленная
стимуляцией диуреза, сопровождается проявлениями гипокалиемии; 3) по
окончании действия маннитола в случае повреждения ГЭБ может проявляться эффект отдачи – вновь
наступающее нарастание отека мозга в связи с возвращением воды из
плазмы крови в ткани. К тому же осмотические диуретики обеспечивают
дегидратацию и уменьшение общего объема мозговой ткани, воздействуя
главным образом на непораженные структуры мозга. Это делает
целесообразным применение его прежде всего при явных признаках
сдавления мозга. Показатели осмотичности крови выше 300 мосм/л и
диурез, превышающий 4-6 л в сут, надо рассматривать как осно- вания для
ограничения дальнейшего применения осмотических диуретиков.
Эффективность
глицерола ниже, чем маннитола: он начинает действовать через 12 ч
после приема внутрь, но практически не вызывает феномена отдачи. Эффективность
приема глицерола отмечается лишь у больных с нерезко вы- раженным
отеком головного мозга, главным образом при ишемическом инсульте.
С целью дегидратации при отеке мозга применяют также салуретики из группы петлевых диуретиков, чаще – фуросемид (лазикс), обычно
по 20-40 мг внутримышечно или внутривенно до 3 раз в день, иногда
целесообразно их сочетание с осмотическими диуретиками (вводят через
3-4 ч после введения маннитола). Фуросемид начинает действовать через
35-105 мин, длительность действия 30 мин-2,5 ч. Показания к назначению петлевых диуретиков: 1)
желательность усиления эффекта, вызываемого осмотическим диуретиком;
2) выравнивание водного баланса в случае выраженного накопления
жидкости в организме; 3) дегидратация при нерезко выраженном отеке
мозга.
Петлевые
диуретики, как и осмотические, также в большей степени воздействуют на
неповрежденные отделы мозга, поэтому профилактическое назначение их при
острых неврологических заболеваниях может оказаться бес-
полезным или даже вредным, так как вызывает нарушение электролитного баланса (снижение содержания калия в крови).
Диакарб (фонурит, ацетазоламид) – это салуретик из группы ингибиторов карбоангидразы, может
применяться вместо фуросемида при явлениях умеренного отека мозга по
250 мг внутрь или через зонд 2-4 раза в день, при этом необходим
контроль за содержанием калия в крови. Начало действия диакарба через 40-120 мин, длительность действия 3-8 ч. В связи с тем, что диакарб подавляет продукцию ЦСЖ, его применение можно признать особенно целесо- образным при интерстициальном варианте отека мозговой ткани.
Кортикостероиды
уменьшают проницаемость ГЭБ, способствуют нормализации проницаемости
мембран и микроциркуляции, блокируют синтез простагландинов и других
веществ, способствующих формированию отека при воспалительных, в
частности инфекционных, процессах, а также и при опухолях мозга. При наличии показаний к применению кортикостероидов обычно назначают дексаметазон в дозе 12-16 мг, в тяжелых случаях 24-48 мг в сут. Начальную его дозу (1/4
суточной) вводят внутривенно, капельно. Повторно препарат назначается
внутривенно или внутримышечно через каждые 6 ч. В очень тяжелых случаях
вводится до 60-100 мг дексаметазона в сутки с постепенным уменьшением
дозы препарата.
При назначении преднизолона следует
учитывать, что его действие более кратковременно, чем дексаметазона;
расчет необходимых доз преднизолона должен производиться исходя из
того, что его терапевтическая активность в сравнении с дексаметазоном в 7 раз меньше. Противопоказанием к назначению кортикостероидов может быть выраженное повышение АД.
При введении больших доз кортикостероидов показано раннее назначение антацидных средств (альмагель
по 2 чайные ложки 4 раза в день или окись магния в порошке по столовой
ложке 4 раза в день и др.) за 15-30 мин до приема пищи естественным
путем или до введения питательной смеси через назогас- тральный зонд.
Применение антацидов направлено на предотвращение желудочных
кровотечений и развития синдрома Мендельсона (абсцедирующая пневмония
вследствие аспирации желудочного сока, если его рН <2).
При длительном применении кортикостероидов возможен ряд побочных явлений и осложнений: замедление
заживления ран, провокация обострения имеющихся инфекционных очагов,
депрессия и психозы, пептические язвы, субкапсулярная катаракта,
остеопороз, признаки синдрома Кушинга. Частота побочных явлений зависит
от характера препарата, его дозы, продолжительности лечения; в целом
она довольно велика и проявляется примерно в 50% случаев при лечении
кортикостероидами. Строго ограничены показания к применению кортикостероидов при гнойном менингите. Их
следует применять лишь при выраженном отеке мозга обычно в качестве
дополнения к внутривенным введениям маннитола (Хартер Д.Х., Петерсдорф
Р.Г., 1997).
Противоотечное действие кортикостероидов обычно проявляется через 12 ч. Кортикостероиды
особенно действенны при вазогенном отеке, обусловленном опухолью
мозга, эффективность их при черепно-мозговой травме, особенно у
взрослых, при кровоизлиянии в мозг, а также при цитотоксическом отеке,
связанном с гипоксией и ишемией мозга, является спорной.
При
лечении кортикостероидами требуется регулярный контроль за содержанием
глюкозы и электролитов в крови для своевременной диагностики иногда
возникающих гипергликемии и гипернатриемии. Возможна целесообразность
параллельного введения антигистаминных препаратов и в некоторых случаях
(для профилактики инфекционных осложнений) антибиотиков.
Больным с отеком мозга, наряду с дегидратацией, необходим
контроль за уровнем вентиляции легких и состоянием центральной
гемодинамики, а также принятие мер по нормализации микроциркуляции и
общего мозгового кровотока.
При отеке мозга больные могут нуждаться в неспецифическом лечении, направленном на нормализацию дыхания (восстановление
проходимости дыхательных путей, обеспечение достаточной оксигенации,
предупреждение и своевременное лечение легочных осложнений), сердечной деятельности, артериального давления. Для облегчения венозного оттока из полости черепа следует приподнять головной конец кровати и установить под углом 15-30?. Необходимы
контроль за состоянием водно-электролитного баланса, КОС и их
коррекция, при этом желательно ограничить количество вводимой жидкости
до 1,5-2 л в сут.
По возможности стоит избегать применения сосудорасширяющих средств:
нитроглицерина,
амиодарона (кордарон), дибазола, антагонистов ионов кальция:
нифедипина (фенигидин, адалат, коринфар, кордипин), а также резерпина,
аминазина, дроперидола, особенно в больших дозах. Проводя дегидратацию,
необходимо одновременно купировать чрезмерную артериальную
гипертензию, проводить соответствующие меры в случае гипертермии,
психомоторного возбуждения, эпилептических припадков. По показаниям
применяют антигипоксанты, метаболически активные средства, в частности
ноотропы, витаминные комплексы.
Клинические проявления и лечебные мероприятия при высоком внутричерепном давлении описаны также в главах 20, 21.
Источник
Схема химиотерапии опухоли головного мозга – Европейские протоколы
а) Общие рекомендации по химиотерапии опухоли головного мозга:
• Перед началом лечения должны быть проверены гематологические показатели, а также функция печени и печек.
• При наличии инфекции химиотерапия не проводится.
• Для женщин: исключить беременность; для мужчин и женщин: консультации в отношении контрацепции.
• Пациент должен лечиться у специалиста с опытом работы в химиотерапии.
• При расчете токсичности обращаться к общим критериям побочных эффектов, в таблице ниже приведены данные о гематологической токсичности.
• Доза определяется с учетом площади поверхности тела (ППТ). У пациентов с расчетной поверхностью тела >2,1 ППТ следует воспринимать как 2,1.
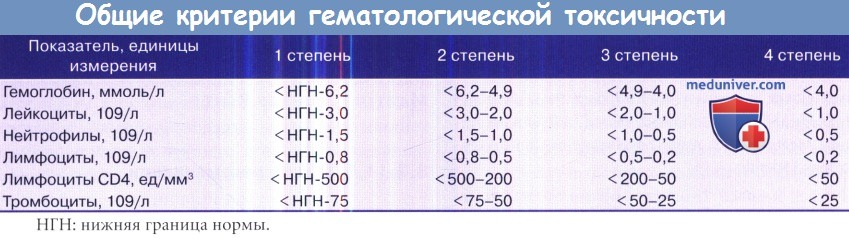
б) Темозоламид:
1. Протокол лучевого лечения с адъювантной и сопутствующей терапией темозоламидом глиом высокой степени злокачественности (протокол EORTC 26981). Лечение состоит из двух этапов: сопутствующей лучевой и химиотерапии темозоломидом, затем шесть циклов классического режима химиотерапии темозоломидом по 1-5 раз в день в течение четырех недель.
I. Темозоламид в сопутствующей фазе. Лучевая терапия (ЛТ) 60 Гр (30×2 Гр) в сочетании с темозоломидом (ежедневно в дозе 75 мг/м2). Предполагаемая продолжительность: шесть недель; сопутствующий прием темозоломида не должен превышать семи недель.
• Прием темозоломида за один час до начала сеанса ЛТ в будние дни. В выходные дни и другие дни без ЛТ прием темозоломида продолжается и проводится в первой половине дня.
• Рекомендуется за час до первой и второй дозы темозоломида прием противорвотного средства (например, 8 мг ондансетрона, 1 мг гранисетрона). При сопутствующей химиолучевой терапии с низкими дозами ТМЗ противорвотная профилактика необходима лишь изредка.
• Профилактика пневмоцистной пневмонии (ПЦП) (960 мг котримоксазола три раза в неделю) показана пациентам, принимающим стероиды в течение сопутствующего этапа, или при CD4 <200/мм3. Профилактика должна продолжаться до полного нивелирования лимфоцитопении (ОКПЭ класса <1).
• Во время лучевой терапии необходимо раз в неделю проверять токсичность.
— Еженедельно: полный анализ крови (гемоглобин, гематокрит, лейкоциты, тромбоциты, CD4-лимфоциты при решении вопроса о профилактике ПЦП).
— В конце четвертой недели и до начала адъювантной терапии: биохимический анализ (функция почек и печени, электролиты, глюкоза).
• Правила отсрочки и отмены приема темозоламида в сопутствующей фазе приведены в таблице ниже.
II. Темозоламид в адъювантной фазе для впервые диагностированных глиом. Первый цикл начинается на 28±3 день после последнего дня лучевой терапии. См. стандартный график приема темозоломида на 1-5 дни каждые четыре недели.
III. Стандартная химиотерапия темозоламидом при рецидивах заболевания или адъювантной терапии:
• Лечение дается в соответствии со стандартным графиком на 1-5 дни каждые четыре недели:
— Начальная доза для первого цикла адъювантной терапии составляет 150 мг/м2/день на 1-5 дни, с однократным повышением дозы до 200 мг/м2/день с первого по пятый дни в последующих циклах в случае отсутствия существенной токсичности в первом цикле (все ОКПЭ без гематологической токсичности <2 класса (за исключением алопеции, тошноты и рвоты) и тромбоцитов > 100 х 109/л и нейтрофилов > 1,5 х 109/л).
— Для лечения рецидивирующих заболеваний:
После предшествовавшей химиотерапии в начале следующего цикла стартовая доза для первого цикла составляет 150 мг/м2 в день на 1-5 дней, с одним повышением дозы до 200 мг/м2/день в последующих циклах в случае отсутствия существенной токсичности. Не получавшим химиотерапии пациенты дают начальную дозу 200 мг/м2/день и темозоламид с первого по пятый дни.
— Используют три уровня дозировок: 200 мг/м2, 150 мг/м2 и 100 мг/м2 ежедневно с первого по пятый день.
• Продолжительность лечения:
— При впервые диагностированной глиоме после сопутствующей химиолучевой терапии не более шести циклов адъювантной терапии.
— При рецидиве заболевания до прогрессирования заболевания или 12 циклов.
• С первого по пятый день стандартного лечения темозоломидом рекомендуется прием противорвотных средств, так как тошнота и рвота могут быть очень серьезными, особенно в первый и второй дни. Так как 5-НТ 3-антагонисты могут вызвать запор, рекомендуется давать ондансетрон (8 мг) или гранисетрон (1 мг) один или два раза в день 1-3 дня, только при необходимости и с приемом за один час до темозоломида.
• Перед каждым циклом лечения темозоломидом должен быть получен общий анализ крови (ОАК) (за 72 ч). Контроль проводится на 21 день первого цикла или после увеличения дозы.
• Снижение дозы на один уровень (обычно примерно на 21-й день) в случае гематологической токсичности 3 или 4 класса или в начале следующего цикла при задержке более трех недель из-за токсичности.
• Лечение прекращают в случае 3-й степени кардиотоксичности, 4-й степени гематологической токсичности или 3-й степени негематологической токсичности в дозе 100 мг/м2 в день (500 мг/м2 за цикл), или негематологической токсичности 4-го класса (за исключением тошноты и рвоты).
• Следующий цикл может начаться, если уровень нейтрофилов > 1,5 х 109/л и/или тромбоцитов >100х 109/л в 29 день = 1-й день следующего цикла, и при отсутствии негематологической токсичности (за исключением алопеции):
— В противном случае — задержка следующего цикла до возникновения указанного состояния.
— Если вопрос не решен в течение трех недель, следует прекратить лечение.
IV. Альтернативные режимы дозирования темозоламида:
• Используются и некоторые другие схемы темозоломида с более плотной дозировкой в течение нескольких дней каждые четыре недели. Наиболее часто используются:
— Неделя через неделю: чередуется одна неделя ежедневного приема и одна неделя отдыха.
• Уровни дозировки: 100 мг/м2 ежедневно, 125 мг/м2 ежедневно, 150 мг/м2 ежедневно.
— Три недели через неделю: три недели ежедневного приема, затем одна неделя отдыха.
• Используется дозировка: 75 мг/м2 ежедневно, 100 мг/м2 ежедневно.
• Тошнота и рвота часто менее выражены, чем при стандартном режиме дозирования.
• Усталость, недомогание и т. д., могут быть более выраженными, усиливаясь после новых циклов.
• Лимфопения является побочным эффектом всех таких режимов. Рекомендуется мониторинг CD4+, с профилактикой ПЦП если CD4+ ниже 200/мм3 (и продолжение до восстановления уровня > 200/мм3).
• Начать с низкой дозы, если перед этим проводилась химиотерапия.
• Уменьшить дозировку и начать новый цикл в соответствии с приведенными рекомендациями в течение 1-5 дней 4 раза в неделю.
• Рассмотреть возможность перехода на стандартное лечение в случае изнурительных общих симптомов.
• Рекомендуемая продолжительность лечения при рецидивирующих опухолях: до одного года.

в) PCV химиотерапия опухоли головного мозга:
• Каждый курс стандартной химиотерапии PCV состоит из:
— CCNU (ломустин), 110 мг/м2 перорально в первый день с противорвотными средствами (метоклопрамид или домперидон, в случае необходимости ондансетрон или аналогичные средства).
— Прокарбазин (натулан), 60 мг/м2 внутрь в течение 14 дней каждого цикла на 8-21 дни.
— Винкристин, 1,4 мг/м2 на 8 и 29 день каждого цикла (максимум 2 мг).
• Полный курс терапии повторяется каждые шесть недель (42 дня), максимум шесть циклов.
• Эффективность винкристина была поставлена под сомнение, и многими врачами этот препарат не включается в схему.
• Токсичность проявляется в основном кумулятивной миелосупрессией, тошнотой, алопецией, повышенной утомляемостью, потерей аппетита, нарушением функции печени и полинейропатией (винкристин).
— Прокарбазин может вызвать аллергическую реакцию кожи.
— Прием тирамин-содержащих продуктов, таких как красное вино, сыр, бананы во время лечения прокарбазином, может вызвать гипертонический криз (эффект моноаминоксидазы). Пациенты должны быть предупреждены о дисульфирам-эффекте после приема алкоголя (головная боль, слабость и потливость).
• Тошнота и рвота, вызванные схемой PCV, как правило, контролируются обычными противорвотными средствами, такими как домперидон или метоклопрамид.
• Контроль показателей:
— Гематологические параметры на 1, 8 и 43 сутки (= 1-й день следующего цикла).
— Биохимический анализ перед началом каждого цикла.
• Модификации дозировки:
— Если схема используется после предыдущей химиотерапии темозоломидом в сочетании с облучением: уменьшить дозу CCNU и прокарбазина на 25%.
— При снижении лейкоцитов <3,0 х 109/л или тромбоцитов <100х 109/л в первый день:
• CCNU задерживается на одну неделю.
В случае последующей лейкопении <3,0×109 или тромбоцитопении <100x 109 лечение откладывается еще на неделю. Если лейкопения или тромбопения сохраняются после этого, необходимо прекратить химиотерапию.
• В случае задержки цикла на две недели из-за токсичности снизить дозировку CCNU и прокарбазина на 25%.
— Уменьшить дозу CCNU и прокарбазина на 25% в случае 3/4 класса лейко- или гранулоцитопении, или в случае 3/4 класса тромбоцитопении.
— В случае уровня лейкоцитов <3,0 х 109/л или тромбоцитов <100 х 109/л на 8-й день:
• Винкристин и прокарбазин откладывают на одну неделю. В случае стойкой лейкопении (<3,0 х 109) или тромбоцитопении (<100 х 109) лечение откладывается еще на неделю. Если гематологические нарушения сохраняются и далее, лечение прекращается.
— Уменьшить дозу CCNU и прокарбазин на 25% в случае 3 степени гематологической токсичности и 2 или 3 степени негематологической токсичности.
— Прекращение лечения в случае:
• 3 степени кардиотоксичности.
• 4 степени гематологической токсичности или 3 степени негематологической токсичности, несмотря на снижение дозы.
• Любой негематологической токсичности 3 степени (за исключением тошноты и рвоты).
— В случае аллергической реакции кожи прием прокарбазина должен быть прекращен.
— Винкристин отменяется в случае 2 степени нейротоксичности.
— В связи с кумулятивной миелосупрессией CCNU продолжение лечения при маргинальных гематологических нарушениях приведет к более высокой токсичности в последующих циклах.
— Как правило, печеночные нарушения постепенно уменьшаются.
г) BCNU (кармустин) для химиотерапии опухоли головного мозга. 60 мг/м2 в 1-3 дни каждые 8 недель:
• Наиболее распространенной схемой для BCNU (кармустина) является 130-200 мг/м2 каждые 6 недель, но 8-недельный прием в дозе 80 мг/м2 оказался эффективным в исследовании на 40 пациентах с глиомами высокой степени злокачественности. Исследование пациентов с мультиформной глиобластомой с предварительным лечением темозоломидом (в комбинации химиолучевой терапии) показало значительную гематологическую токсичность при такой дозировке и снижении дозировки до 60 мг/м2 в 1-3 день восьминедельного цикла.
• Основные побочные эффекты: гематологическая токсичность, токсическое поражение печени, тошнота и легочная токсичность.
• BCNU вводят внутривенно с первого по третий день в дозе 60 мг/м2/день (доза на цикл 180 мг/м2) каждые 8 недель. Назначают противорвотные средства (метоклопрамид, домперидон).
• Противопоказания: заболевания легких в анамнезе, так как возможно действие на функцию легких; необходимо оценить функцию по диффузионной емкости оксида углерода, которая должна быть выше 60% прогнозируемого значения.
• Контроль показателей:
— Гематологические параметры на 21, 28, 35, 42, 65 сутки (= первый день следующего цикла).
— Биохимический анализ перед началом каждого цикла.
• Модификации дозировки:
— В случае количества лейкоцитов <3,0 х 109/л или тромбоцитов <100 x 109/л в первый день—задержка до восстановления.
• Если гематологическая токсичность не регрессирует в течение двух недель или повторяется токсичность 2 степени в ходе последующего цикла, следует прекратить лечение.
— В случае гематологической токсичности 3-й степени дозировка для следующего цикла снижается на 25%.
— В случае гематологической токсичности 4 степени дозировка для следующего цикла снижается на 50%.
— При негематологической токсичности:
• Не начинать следующий цикл, пока вся токсичность (за исключением алопеции) не регрессирует до 1 степени или менее.
• При печеночной токсичности 2 степени дозировка следующего цикла снижается на 25% после возвращения к нормальным показателям.
• При печеночной токсичности 3 степени дозировка следующего цикла снижается на 50% после возвращения к нормальным показателям.
• В случае легочной токсичности 3 или 4 степени лечение следует прекратить.
• В случае любой негематологической токсичности 4 степени или непеченочной токсичности 3 степени (за исключением тошноты, рвоты и алопеции) лечение необходимо прекратить.
• Если негематологическая токсичность не восстанавливается в течение первого месяца или если негематологическая токсичность повторяется в последующем цикле до степени >2, следует прекратить лечение.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
– Также рекомендуем “Схема адъювантного лечения опухоли мозга у ребенка – Европейские рекомендации”
Оглавление темы “Нейрохирургия опухоли головного мозга.”:
- Схема лучевой терапии опухоли головного мозга – Европейские рекомендации
- Схема химиотерапии опухоли головного мозга – Европейские протоколы
- Схема адъювантного лечения опухоли мозга у ребенка – Европейские рекомендации
- Схема адъювантной терапии злокачественной глиомы головного мозга у ребенка – Европейские рекомендации
- Схема адъювантной терапии медуллобластомы у ребенка – Европейские рекомендации
- Схема адъювантной терапии эпендимомы у ребенка – Европейские рекомендации
- Новые методы лечения опухоли головного мозга и их эффективность
- Алгоритм диагностики аневризмы сосуда головного мозга – Европейские рекомендации
Источник
