Отек легких на фоне пароксизма фибрилляции предсердий

Оглавление темы “Фибрилляции предсердий – диагностика, лечение.”:
- Признаки мерцания предсердий на ЭКГ
- ЭКГ при фибрилляции предсердий (ФП)
- Причины фибрилляции предсердий и их прогноз
- Классификация фибрилляции предсердий
- Шкалы риска тромбоэмболии при фибрилляции предсердий
- Фибрилляция предсердий. Лечение пароксизма фибрилляций предсердий
- Антикоагулянты для профилактики тромбоэмболии при фибрилляции предсердий
- Лечение фибрилляции предсердий стратегией контроля частоты
- Лечение фибрилляции предсердий стратегией контроля ритма
- Лечение рефрактерной (стойкой) фибрилляции предсердий
Фибрилляция предсердий. Лечение пароксизма фибрилляций предсердий
Фибрилляция предсердий (ФП) (с частотой сокращения желудочков более 150 уд/мин) — маркер плохого прогноза и независимый фактор, повышающий внутрибольничную летальность.
Пароксизм фибрилляции предсердий (ФП) связан с тяжелым поражением ЛЖ (обширным ИМ) и наличием СН (со значимыми гемодинамическими проявлениями).
Фибрилляция предсердий обусловлена появлением микро «re-entry» в предсердии, встречается при ИМ в 10-15% случаев (у пожилых лиц в 2—3 раза выше). Ранняя (в первые сутки ИМ) ФП носит, как правило, преходящий характер.
В более поздние сроки появление фибрилляции предсердий (ФП) связано с растяжением левого предсердия у больных с выраженной дисфункцией ЛЖ, перикардитом или ишемическим повреждением предсердий. Пароксизм ФП может вызвать смерть у 25% больных на фоне обширного ИМ передней локализации, особенно при ЧСС более 160 уд/мин или при большом дефиците пульса, когда мал выброс крови в аорту.
Появление фибрилляции предсердий (ФП) повышает летальность при ИМ в 2 раза, поэтому ее надо быстро купировать.
Прогностическое значение фибрилляций предсердий при инфаркте миокарда определяется частотой сокращения желудочков, размерами ЛПр и временем купирования приступа.
В период пароксизма тахисистолической формы фибрилляций предсердий могут усилиться ишемия и ИМ, возникнуть серьезные гемодинамические последствия (аритмогенный КШ, ОЛЖН, снижение мозгового кровотока) не только вследствие быстрого и малоэффективного сокращения желудочков, но и из-за потери транспортной функции предсердиями.
Появление фибрилляции предсердий (ФП) на фоне ИМ часто чревато системной эмболизацией инсультами и летальностью, особенно у больных с ИМ передней стенки.
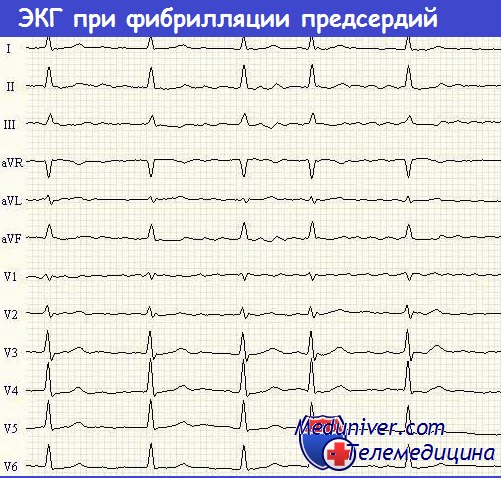
ЭКГ при фибрилляции предсердий
Лечение пароксизма фибрилляций предсердий на фоне ИМ проводится по общим правилам При хорошей переносимости и отсутствии тахисистолии можно воздержаться от специального лечения, так как СР часто восстанавливается спонтанно.
При плохой переносимости фибрилляции предсердий (ФП) проводят электрическую кардиоверсию (но велика вероятность возобновления ФП) или внутривенно вводят амиодарон (лучший препарат для купирования ФП при ИМ), который в последующем назначают в течение 6 недель для снижения риска повторного развития фибрилляции предсердий (ФП).
Показания к экстренному восстановлению сердечного ритма с помощью электроимпульсной терапии выраженные нарушения гемодинамики (больной задыхается, не может лежать, а сидит, имеется гипотензия), рецидивирующие боли в сердце, расширение зоны инфаркта или ишемии. В этом случае нельзя терять время, так как возможно быстрое развитие отека легких.
При фибрилляции предсердий и трепетании предсердий имеется высокая частота сокращения желудочков и гипотензия, что способствует расширению зоны некроза миокарда Лечение этих наджелудочковых тахиаритмий должно быть быстрым, особенно если частота сокращений желудочков более 100 уд/мин.
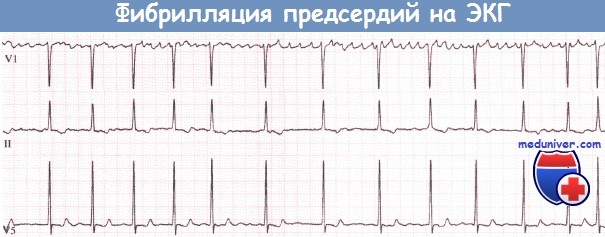
Фибрилляция предсердий (ФП): волны f отчетливо проявляются в отведении V1, едва заметны в отведении II и не видны в отведении V5.
При стабильном состоянии больного и отсутствии выраженных нарушений гемодинамики проводят фармакологическую терапию.
Первый шаг (когда восстановление сердечного ритма не показано) — урежение частоты сокращения желудочков при высокой исходной тахикардии и перевод тахисистолической формы ФП в брадисистолическую (с частотой сокращения желудочков менее 60 уд/мин).
Используют внутривенно антиаритмические препараты, блокирующие проведение импульса в АВ-узле пропранолол, амиодарон, дигоксин и с осторожностью — верапамил (из-за его кардиодепрессивного действия).
Дигоксин и амиодарон являются препаратами выбора у больных с наличием явной сердечной недостаточности (СН). Вводят:
• Амиодарон — по 300—400 мг (5 мг/кг) без разведения за 5— 10 мин, суточная доза до 1200 мг;
• Адреноблокаторы (уменьшающие ишемию миокарда и симпатический тонус) — пропранолол (внутривенно по 5 мг за 5 мин) тиметопролол (болюс— 5 мг, затем каждые 5—10 мин до достижения общей дозы 20 мг), потом его же назначают внутрь (каждые 6 ч по 25—50 мг). Бета-адреноблокаторы не показаны при тяжелой СН и ХОБЛ.
В отсутствие противопоказаний большая часть больных может после перенесенного ИМ принимать амбулаторно АБ (снижающие частоту сокращений желудочков и рецидивы ФП);
• Сердечные гликозиды, единственное показание для назначения которых при ИМ — это пароксизмы фибрилляций предсердий. Дигоксин вводят внутривенно болюсом в насыщающей дозе по 1 мг (0,6—1 мг для больного с массой тела 70 кг) за 5 мин. Но начало эффекта дигоксина проявляется лишь через несколько часов.
В ряде случаев дигоксин в малой дозе добавляют к бета-адреноблокатору (удлиняющим рефрактерность АВ-узла), если у больного имеется быстрый желудочковый ритм и легкая ХСН.
При отсутствии эффекта (но после урежения сокращения желудочков), через 1 час для восстановления сердечного ритма (это не всегда надо) вводят амиодарон;
• всем больным с фибрилляциями предсердий показано внутривенное введение гепарина (доза зависит от длительности фибрилляций предсердий). Так, при длительности ФП более 48 ч необходим прием антикоагулянтов, особенно при крупноочаговых передних ИМ. Больной с повторными эпизодами ФП должен принимать оральные антикоагулянты (чтобы снизить риск развития инсульта), даже если у него имеется СР при выписке из больницы.
Учебное видео ЭКГ при суправентрикулярной тахикардии (синусовой тахикардии, фибрилляции предсердий, трепетании предсердий)

– Также рекомендуем “Шкалы риска тромбоэмболии при фибрилляции предсердий”
Источник
23 января 20192532,1 тыс.
Пароксизмальная мерцательная аритмия — что это такое? Патология с характерными нарушениями согласования сократительных движений мышечного волокна миокарда. Достаточно распространена, но как самостоятельное явление диагностируется редко, в основном выступая косвенным признаком болезней сердца, сосудистой и дыхательной систем.
Пароксизмальная мерцательная аритмия выражается в периодических сбоях в работе синусового узла, при которых миоциты предсердий колеблются в хаотичном порядке (частота доходит до 400 сокр./мин). То есть из 4 сердечных камер свои функции продолжают выполнять только желудочки, что отрицательно сказывается на работе всей системы кровотока.
Причины появления пароксизмальной формы
Пароксизмальная мерцательная аритмия (ПМА) — код по МКБ 10:
- I00-I99 класс IX (болезни системы кровообращения),
- I30-I52 (другие заболевания сердца),
- I48 (фибрилляция и трепетание предсердий).
Основная причина ПМА одна — это болезни сердца и сосудов:
- ишемия сердца;
- гипертония;
- все формы сердечной недостаточности;
- миокардиты, эндокардиты, перикардиты и прочие нарушения работы сердца, спровоцированные воспалением;
- приобретенный и врожденный порок сердца (при расширении камер);
- генетические кардиомиопатии (гипертрофическая и дилатационные).
Предрасполагающие факторы
К сторонним провоцирующим факторам относятся:
- злоупотребление табаком и алкоголем, стимулирующими наркотиками;
- нарушения электролитного баланса с магние-калиевым дефицитом;
- структурные патологии органов и тканей дыхательной системы.
- инфекционная инвазия в острой форме;
- послеоперационные состояния;
- патологии эндокринной системы;
- терапия адреномиметиками, сердечными гликозидами;
- хронические стрессы.
Пароксизм мерцательной аритмии, проявившийся при неустановленных причинах, называется идиопатическим.
Формы и виды пароксизмальной мерцательной аритмии
Пароксизмальная форма мерцательной аритмии — нарушение работы сердечной мышцы, длящееся максимум неделю. Если измененное состояние длится дольше, кардиологи диагностируют хроническую форму.
В зависимости от частоты сокращений предсердий
- Типичное мерцание при частоте более 300 сокр./мин.
- Показательное трепетание при частоте не выше 200 сокр./мин.
От частоты сокращения желудочков
Независимо от того, насколько правильно работают предсердия, к желудочкам доходит не каждый проводящий импульс. По частоте сокращения желудочков ПМА можно классифицировать на:
- брадисистолическую форму: частота менее 60 сокр./мин;
- тахисистолическую: частота более 90 сокр/мин;
- нормосистолическую или промежуточную, с вариативной частотой.
По локализации
Относительно локализации очагов повышенного формирования импульса различается 3 типа пароксизма при мерцательной аритмии:
- аритмия предсердий — импульсы формируются в предсердном узле;
- аритмия желудочков — импульсы зарождаются в проводящей системе желудочков;
- смешанная аритмия — с несколькими патологическими очагами.
По клиническому течению
Самая распространенная — промежуточная форма нарушений ритма. Повторяющиеся ПМА приступы расцениваются как рецидивирующая аритмия.
Симптомы и проявления болезни
Тяжесть симптоматики напрямую зависима от частоты желудочковых сокращений. Незначительные отклонения от нормы (90-100 сокр./мин) не проявляются наглядно.
Тахисистолическая форма, диагностируемая чаще всего, имеет следующие признаки:
- чувство «замирания» сердца, ощутимые перебои;
- частое сердцебиение;
- неравномерный пульс;
- одышка в состоянии покоя, усиливающаяся при физических нагрузках;
- поверхностное дыхание, задержка вдоха при горизонтальном положении, головокружение;
- боли за грудиной;
- обморочные состояния, мышечная атония;
- испарина, гипергидроз;
- панические атаки.
Критическое снижение частоты сокращений приводит к гипоксии и ухудшению мозгового кровоснабжения. Больной получает обморок, иногда он сопровождается остановкой дыхания. Это неотложное состояние, требующее срочных реанимационных мероприятий.
Методы диагностики
С целью уточнения предварительного диагноза кардиолог выслушивает сердечные ритмы. Констатируется аритмия, кроме случаев, когда трепетание приходится на каждое 2, 3 или 4 сокращение.
В такой ситуации признают правильную форму МА и назначают пациенту ЭКГ. Кардиограмма — метод выбора при диагностике патологичных изменений ритма.
Как дополнительный диагностический метод применяют УЗИ сердца с ЭХО-КГ. Дифференциально важные параметры: размер предсердий, степень износа клапанов. От полученных результатов зависит выбор тактики лечения.
Основы лечения болезни
Мерцательная пароксизмальная аритмия, лечение которой возможно только в условиях стационара, опасна изменчивой картиной течения. Выбор методик основывается на сроке давности приступа:
- если он был менее 2 суток назад, то стараются восстановить ритм (синусовый);
- если прошло более 2 суток, то увеличивается риск эмболии, вызванной восстановлением ритма.
Как вспомогательное средство используют «Варфарин», обладающий свойствами антикоагулянта. Разжижение крови должно воспрепятствовать появлению тромбирующих сосуды сгустков. Восстановление ритма начинают не ранее, чем через 3 недели.
Для контроля состояния пациента применяют чрезпищеводное УЗИ, в ходе которого устанавливают факт наличия/отсутствия сгустков в предсердии. Больные с отрицательным результатом переводятся на интенсивный цикл лечения без ожидания предписанных 3 недель. При таком подходе риск эмболии минимизирован.
Медикаментозное лечение
Фармацевтика предлагает несколько основных средств для купирования приступов ПМА:
- на основе новокаина — снижает давление;
- на основе дигоксинов — с целью контроля частоты сокращений;
- «Кордарон», «Пропаном» — для приема в домашних условиях.
Препараты для внутривенных инъекций вводятся только под контролем врача. Неотложные мероприятия при пароксизме мерцательной аритмии купируют приступ с вероятностью в 95%.
Электроимпульсная терапия
Если медикаментозное лечение не принесло положительных результатов, то больной направляется на курс терапии с использованием электрического разряда.
Электроимпульсная терапия назначается также при наличии осложнений, ставших последствиями приступов пароксизма.
Что это дает пациенту? Происходит перезапуск проводящей системы, ритм стабилизируется благодаря возбуждению синусового узла.
Хирургическое лечение
При рецидивирующей мерцательной аритмии пациент направляется на хирургическую операцию. Используют лазер, прижигая патологический очаг возбуждения в миокарде.
Для выполнения процедуры при помощи нескольких катетеров делается артериальный прокол. Результативность операции по методу радиочастотной абляции (РЧА) составляет около 85%. Если первая операция не была успешной — процедуру проводят повторно.
Первая помощь при пароксизме мерцательной аритмии
Пароксизм мерцательной аритмии — неотложная помощь при мерцании предсердий:
- внутривенное введение «Аймалина» и/или «Новокаинамида», «Ритмилена». Противопоказания — нарушения гемодинамики, отек легких, резкое снижение АД;
- если введение вышеуказанных препаратов невозможно, прибегают к электроимпульсному воздействию;
- снижают частоту желудочкового ритма средствами на основе дигоксина или используют «Изоптин», «Верапамил», «Финотипин». Противопоказания — артериальная гипотония.
Догоспитальный этап не предполагает купирования длительных приступов пароксизма, больной госпитализируется. При невысокой частоте желудочковых сокращений тактика неотложной помощи должна быть активной, с назначением пероральных препаратов «Пропранолол» и/или «Хинидин».
Пароксизм мерцательной аритмии — неотложная помощь трепетании предсердий:
- Гемодинамика при трепетании практически неизменна в сравнении с нарушениями при мерцании. Пациент может вовсе не ощущать симптомов аритмии. Экстренная помощь не предусмотрена и переходят к плановому лечению;
- Если гемодинамические нарушения все же проявились, что выражается в тупой боли в грудине, используют препараты, снижающие частоту ритма, например, «Верапамил» или «Пропранолол». Противопоказания — артериальная гипертония и острая сердечная недостаточность;
- В 10% случаев купировать трепетание предсердий можно только при помощи электроимпульсного воздействия.
Возможные осложнения
Пароксизмальная мерцательная аритмия, неотложная помощь при которой была проигнорирована или оказана не в полной мере, приводит к изменениям интенсивности кровотока. Что, в свою очередь, становится причиной эмболии в полости предсердий. Кроме того, отказ от врачебной помощи спровоцирует:
- отек легких на фоне острой сердечной недостаточности. Усугубляет нарушения ритма;
- гипоксический шок с характерным снижением давления и нарушениями транспортировки кислорода к внутренним органам. Развивается как следствие критически высокой (более 150 сокр./мин) или критически низкой (меньше 40 сокр./мин) частоты желудочкового трепетания;
- остановку сердца;
- обморок;
- патологическое изменение коронарного кровотока, с риском возникновения стенокардии и развития инфаркта.
Пароксизм мерцательной аритмии: что это такое — тромбоэмболические осложнения?
Опасность тромбоэмболии становится серьезней, если с момента приступа прошло более двух суток.
За это время в предсердии образуются сгустки внушительного размера. Тромбы попадают в головной мозг, конечности и сердце, что приводит к инфаркту, инсульту или гангрене.
Прогноз и профилактика болезни
Прогноз жизни при этой болезни достаточно благоприятен. Важнее всего контролировать частоту сокращений, поддерживая ее в рамках возрастной нормы. Не менее действенна и профилактика тромбоэмболии.
Купирование частых приступов требует профилактики образования тромбов посредством приема «Варфарина», являющегося дополнением к антиаритмическому лечению и антагонистом витамина К.
Контрольный анализ крови сдается пациентом раз в месяц, показателем успешности терапии выступает МНО (международное нормализованное отношение), поддерживаемое на уровне 2,5-3,5.
Рекомендуемые профилактические мероприятия:
- Лечение патологий, приведших к аритмии.
- Восполнение дефицита магния и калия.
- При патологии нервной системы, на фоне которой развивается пароксизмальная мерцательная аритмия:
- физическая нагрузка снижается до минимума, назначается диета, лечение запоров и ожирения, подавляется активность блуждающего нерва (вагусный тип вовлечения нервной системы);
- предупреждается эмоциональное напряжение, назначаются успокоительные, увеличивается продолжительность отдыха, вводятся ограничения на употребление кофеиносодержащих напитков, табака, полезны щадящие занятия ЛФК (гиперадренэргический тип вовлечения нервной системы).
Полезное видео
Чем чревато несвоевременное начало лечения мерцательной аритмии и более подробная информация об этом заболевании – все это есть в следующем видеосюжете:
Приступы мерцательной аритмии случаются практически у всех. Первое, что должен сделать пострадавший — обратиться за неотложной медицинской помощью, вне зависимости от силы и проявлений пароксизма. Критически важно восстановить синусовый ритм в первые 2 суток после приступа, это поможет предупредить развитие эмболии.
Источник
Фибрилляция предсердий (ФП) — нозология, заслуживающая отдельного внимания среди всех нарушений ритма сердца. Это обусловлено ее высоким преваленсом в популяции (около 3% у людей старше 20 лет) [1, 2], наибольшим среди пациентов пожилого возраста, а также с сопутствующими заболеваниями, такими как артериальная гипертензия (АГ), сердечная недостаточность (СН), ишемическая болезнь сердца (ИБС), ожирение, сахарный диабет (СД) и хроническая болезнь почек (ХБП) [3]. Каждый третий инсульт [4, 5] и каждая третья госпитализация с СН [6] обусловлены ФП. Наличие ФП увеличивает в 1,5–2 раза риск смерти от всех причин [7] и значительно снижает качество жизни [8].
Признаками острого коронарного синдрома (ОКС), возникшего вследствие атеротромбоза коронарных артерий (КА), являются острая боль в грудной клетке, ишемические изменения ЭКГ, повышение уровня сердечного тропонина [8]. Общеизвестно, что при тахиаритмии, такой как ФП с быстрым ответом желудочков, эти явления могут иметь место и при отсутствии как атеротромбоза, так и значимого атеросклероза коронарных артерий (АКА), особенно при остром развитии нарушения ритма сердца [9–11]. Однако вопрос отграничения друг от друга этих состояний остается открытым. Тем не менее, по данным большинства авторов, у всех пациентов с ФП вероятность АКА выше, чем в популяции [12, 13]. Современные эпидемиологические исследования указывают на широкий диапазон встречаемости ангиографически верифицированного АКА у пациентов с ФП — от 36% до 82% [14–17]. При этом встречаемость ФП у пациентов с ОКС ниже этих значений и варьирует от 5% до 23% [18, 19]. Таким образом, актуальным представляется вопрос — у кого из пациентов с пароксизмом ФП и признаками ишемии миокарда может быть обнаружен АКА и имеет ли этот факт какое-либо значение?
Материалы и методы исследования
Вид исследования — проспективное, открытое, выборочное. Период наблюдения составил 12 месяцев. Включено 75 пациентов в возрасте 65,8 ± 8,1 года, из них 31 мужчина (41,3%), госпитализированных в кардиологическое отделение с пароксизмом ФП в сочетании с признаками острой ишемии миокарда (болью в груди, повышением уровня тропонина и изменениями ЭКГ, за исключением стойкой элевации сегмента ST), на основании которых диагностировались нестабильная стенокардия (НС) или инфаркт миокарда (ИМ) без подъема ST. Всем пациентам для восстановления синусного ритма выполнена электрическая кардиоверсия по неотложным показаниям. Ведение пациентов осуществлялось в полном соответствии с рекомендациями Европейского общества кардиологов (European Society of Cardiology, ESC) и Российского кардиологического общества.
Критериями исключения являлись: перманентная и хроническая ФП (> 48 часов), ИМ с элевацией сегмента ST, невозможность проведения коронарной ангиографии (КАГ), гемодинамически значимые пороки сердца, нарушение функции щитовидной железы, тяжелая обструктивная патология бронхов, онкологические, аутоиммунные или системные воспалительные болезни, тяжелая печеночная или почечная недостаточность.
По данным ЭКГ оценивалось наличие ФП, девиации сегмента ST и изменений волны Т. Ишемической считалась нисходящая или горизонтальная депрессия ST ≥ –0,1 mV. Ишемическими изменениями Т считались ее уплощение (амплитуда от +0,1 до –0,1 mV) или инверсия (амплитуда ≥ –0,1 mV). Эхокардиография (Эхо-КГ) выполнялась трансторакальным доступом по стандартной методике. Систолическую дисфункцию определяли как снижение менее 50% фракции выброса (ФВ) левого желудочка (ЛЖ) по методу Симпсона. Всем пациентам выполнена КАГ. Значимым атеросклероз считался при наличии стеноза ≥ 50% хотя бы одной КА (передней нисходящей, огибающей, правой или их крупных ветвей).
По результатам КАГ пациенты разделены на 2 группы: 1-я группа — 28 пациентов в возрасте 67,2 ± 8,1 года, 18 мужчин (64,2%), со значимым АКА, 2-я группа — 47 пациентов в возрасте 64,9 ± 8,1 года, 13 мужчин (27,7%), с интактными КА.
Выполнен анализ чувствительности, специфичности и диагностической эффективности клиники, изменений ЭКГ и повышения уровня тропонина в прогнозировании АКА у пациентов с пароксизмом ФП и признаками ишемии миокарда.
Проведена оценка госпитального прогноза: частоты смерти, развития ИМ, стентирования КА, коронарного шунтирования (КШ). Проведена оценка долгосрочного прогноза: частоты смерти, развития ИМ, стентирований КА, КШ, кровотечений, инсульта за 12 месяцев наблюдения.
Статистическую обработку данных осуществляли с использованием программ MS Excel, Biostat 2009. Для оценки характера нормальности распределения данных применяли критерий Шапиро–Уилка. Распределение в выборке нормальное, применялись методы параметрической статистки. Данные представлены в виде среднего значения и стандартного отклонения. Различие между количественными признаками оценивалось с помощью критерия Стьюдента. Для выявления взаимосвязей между качественными признаками использовался анализ распределения с помощью критерия χ2. Различия между группами считались статистически значимыми при р < 0,05.
Результаты и их обсуждение
Наличие хотя бы одного признака острой коронарной недостаточности при поступлении было обязательным для включения. В табл. 1 представлены общие сведения о всех пациентах. Значимый АКА выявлен у 37,3% из них, что соответствует данным представленных выше эпидемиологических исследований [14–17].
.gif)
Возрастная категория, встречаемость ангинозной боли, изменений ЭКГ и повышения уровня тропонина в группах пациентов с АКА и без него не отличались. В группе с АКА превалировали мужчины (р = 0,004), что неудивительно — мужской пол является одним из классических немодифицируемых факторов риска атеросклероза [8]. Диагностированные ранее нозологии, в основе которых лежит атеросклероз или атеротромбоз в любом артериальном бассейне, увеличивают вероятность наличия у пациента АКА [8] — у пациентов группы АКА в 6 раз чаще имелось указание в анамнезе на перенесенный ИМ (39,3% против 6,4%, р = 0,001).
Однако на этом различия между исследуемыми группами заканчиваются. Ожирение, курение, диагностированные ранее стенокардия напряжения, СН, ХБП, АГ, СД, дислипидемия, болезнь периферических артерий, транзиторная ишемическая атака и нарушение мозгового кровообращения встречались с одинаковой частотой у пациентов с АКА и без него.
Трансторакальная Эхо-КГ рекомендована всем пациентам с ФП для исключения органической патологии сердца и выбора тактики ведения [20]. Нередкой находкой у таких пациентов являются диастолическая и/или систолическая дисфункция ЛЖ [21]. По результатам Эхо-КГ наших пациентов в группе АКА чаще в 4,5 раза выявлялись нарушения локальной сократимости миокарда (39,3% против 8,5%, р = 0,003) и в 10 раз чаще систолическая дисфункция ЛЖ (21,4% против 2,15%, р = 0,018). Сведения о клинической картине, данных анамнеза и результатах Эхо-КГ представлены в табл. 2.
.gif)
Депрессия ST и изменения зубца Т встречаются примерно у 50% пациентов с ИМ без подъема ST и НС [22]. Считается, что изменения зубца Т чувствительны, но не специфичны для острой ишемии миокарда [23]. Выявленная в динамике от предыдущих ЭКГ девиация ST — специфичный и наиболее важный признак ишемии миокарда, а также значимый прогностический критерий. Однако в случае развития ФП с быстрым ответом желудочков увеличение частоты сердечных сокращений и как следствие рост потребности миокарда в кислороде, а также укорочение диастолы и уменьшение коронарной перфузии [8] могут приводить к развитию ишемии и повреждения миокарда и появлению соответствующих изменений ЭКГ, в том числе при отсутствии АКА [24, 25].
Показатели диагностической эффективности в прогнозировании АКА у пациентов с пароксизмом ФП «трех китов» диагностики ОКС (клиническая картина, девиация ST и изменения зубца Т, маркеры некроза миокарда) в целом оказались невысоки и составили: у ангинозной боли Se = 75%, Sp = 36,2%, ИДЭ = 50,7%, у изменений ЭКГ Se = 67,9%, Sp = 38,3%, ИДЭ = 49,3% и уровня тропонина Se = 32,1%, Sp = 87,2%, ИДЭ = 66,7%. Наибольшей диагностической эффективностью обладало сочетание ангинозной боли и изменения уровня тропонина — Se = 50%, Sp = 63,8%, ИДЭ = 69,3%. Данные представлены в табл. 3.
.gif)
Данные наиболее крупных регистров ОКС (GRACE/GRACE2, CANRACE, SWEDENHEART, CAMI) согласуются между собой в отношении частоты проведения КАГ и реваскуляризации миокарда у пациентов с ФП. По сравнению с пациентами без ФП, им в рамках ОКС в 1,5 раза реже выполняется КАГ, а в случае выявления АКА в 1,8 раза реже проводится ангиопластика со стентированием КА и КШ [26–28], несмотря на то, что большинство исследователей рассматривают ФП при ОКС как фактор неблагоприятного прогноза. Так, по результатам регистра ARIAM (2001–2011 гг.) новый эпизод ФП у пациента с ОКС ассоциирован с двукратным увеличением госпитальной летальности. По данным регистра SWEDENHEART (2000–2009 гг.) у пациентов с ФП, независимо от ее типа, cмертность выше на 59%, а развитие ИМ — на 14%. По данным крупного метаанализа (1970–2009 гг.) ФП при ИМ является независимым предиктором смерти — впервые возникшая аритмия увеличивает риск на 37%, имеющаяся в анамнезе — на 28% [29].
Прогностические параметры наших пациентов представлены в табл. 4. Очевидно, что пациентам со значимым АКА чаще выполнялось стентирование КА за период госпитализации. В частоте развития ИМ и смерти, выполнения КШ в остром периоде достоверных различий между группами получено не было. Однако суррогатный показатель в виде комбинированной конечной точки (диагностированный ИМ, реваскуляризация миокарда и смерть во время госпитализации) оказался выше в 6 раз в группе пациентов с пароксизмом ФП и АКА (78,6% против 12,8%, р < 0,001). Аналогичным образом события развивались и в течение 12 месяцев наблюдения. Группы не различались отдельно по частоте развития ИМ, кровотечений, инсульта, смерти и реваскуляризации миокарда. Тем не менее общее число событий также оказалось выше в группе пациентов с АКА (46,4% против 10,6%, р = 0,001).
Выводы
- Значимый коронарный атеросклероз имел место у трети пациентов с ишемическими симптомами на фоне пароксизма фибрилляции предсердий.
- Коронарный атеросклероз у пациентов с пароксизмом фибрилляции предсердий и признаками ишемии миокарда позволяет предположить мужской пол, перенесенный инфаркт миокарда, а также наличие нарушений локальной сократимости и снижения систолической функции миокарда левого желудочка.
- В прогнозировании атеросклероза коронарных артерий у пациентов с пароксизмом фибрилляции предсердий и ишемическими симптомами наибольшей чувствительностью обладает ангинозная боль, наибольшей специфичностью — ее сочетание с повышением уровня тропонина и/или изменениями ЭКГ, наибольшей диагностической эффективностью — сочетание боли в груди и изменения уровня тропонина.
- Выявление коронарного атеросклероза у пациентов с пароксизмом фибрилляции предсердий в сочетании с признаками ишемии миокарда может иметь важное клиническое значение, поскольку по результатам нашего исследования это обусловливало худший госпитальный и долговременный прогноз.
Литература
- Bjorck S., Palaszewski B., Friberg L. et al. Atrial fibrillation, stroke risk, and warfarin therapy revisited: a population-based study // Stroke. 2013. Vol. 44. P. 3103–3108.
- Haim M., Hoshen M., Reges O. et al. Prospective national study of the prevalence, incidence, management and outcome of a large contemporary cohort of patients with incident non-valvular atrial fibrillation // J Am Heart Assoc. 2015. Vol. 4. e001486.
- Zoni-Berisso M., Lercari F., Carazza T. et al. Epidemiology of atrial fibrillation: European perspective // Clin Epidemiol. 2014. Vol. 6. P. 213–220.
- Andersson T., Magnuson A., Bryngelsson I. L. et al. All-cause mortality in 272,186 patients hospitalized with incident atrial fibrillation 1995–2008: a Swedish nationwide long-term case control study // Eur Heart J. 2013. Vol. 34. P. 1061–1067.
- Stewart S., Hart C. L., Hole D. J. et al. A population-based study of the longterm risks associated with atrial fibrillation: 20-year follow-up of the Renfrew/ Paisley study // Am J Med. 2002. Vol. 113. P. 359–364.
- Kotecha D., Holmes J., Krum H. et al. Efficacy of beta blockers in patients with heart failure plus atrial fibrillation: an individual-patient data meta-analysis // Lancet. 2014. Vol. 384. P. 2235–2243.
- McManus D. D., Rienstra M., Benjamin E. J. An update on the prognosis of patients with atrial fibrillation // Circulation. 2012. Vol. 126. e143–146.
- Mann D., Zipes D., Libby P., Bonow R. Braunwald’s Heart Disease: A Textbook of Cardiovascular Medicine, International Edition, 10th Edition. Elsevier Science, 2014. 2040 p.
- Gupta K., Pillarisetti J., Biria M. et al. Clinical utility and prognostic significance of measuring troponin I levels in patients presenting to the emergency room with atrial fibrillation // Clin Cardiol. 2014. Vol. 37, № 6. P. 343–349.
- Lippi G., Picanza A., Formentini A. et al. The concentration of troponin I is increased in patients with acute-onset atrial fibrillation // Int J Cardiol. 2014. Vol. 173. P. 579–580.
- Parwani A. S., Boldt L. H., Huemer M. et al. Atrial fibrillation-induced cardiac troponin I release // Int J Cardiol. 2013. Vol. 168, № 3. P. 2734–2737.
- Nucifora G., Schuijf J. D., van Werkhoven J. M. et al. Relationship between obstructive coronary artery disease and abnormal stress testing in patients with paroxysmal or persistent atrial fibrillation // Int J Cardiovasc Imaging. 2011. Vol. 27, № 6. P. 777–785.
- Weijs B., Pisters R., Haest R. J. et al. Patients originally diagnosed with idiopathic atrial fibrillation more often suffer from insidious coronary artery disease compared to healthy sinus rhythm controls // Heart Rhythm. 2012. Vol. 9, № 12. P. 1923–1929.
- Androulakis A., Aznaouridis K. A., Aggeli C. J. et al. Transient ST-segment depression during paroxysms of atrial fibrillation in otherwise normal individuals: relation with underlying coronary artery disease // J Am Coll Cardiol. 2007. Vol. 50. P. 1909–1911.
- Askew J. W., Miller T. D., Hodge D. O. et al. The value of myocardial perfusion single-photon emission computed tomography in screening asymptomatic patients with atrial fibrillation for coronary artery disease // J Am Coll Cardiol. 2007. Vol. 50. P. 1080–1085.
- Goto S., Bhatt D. L., Rother J. et al. Prevalence, clinical profile, and cardiovascular outcomes of atrial fibrillation patients with atherothrombosis // Am Heart J. 2008. Vol. 156. P. 855–863.
- Lloyd-Jones D. M., Wang T. J., Leip E. P. et al. Lifetime risk for development of atrial fibrillation: the Framingham Heart Study // Circulation. 2004. Vol. 110. P. 1042–1046.
- Lau D. H., Huynh L. T., Chew D. P. et al. Prognostic impact of types of atrial fibrillation in acute coronary syndromes // Am J Cardiol. 2009. Vol. 104. P. 1317–1323.
- Wong C. K., White H. D., Wilcox R. G. et al. New atrial fibrillation after acute myocardial infarction independently predicts death: the GUSTO-III experience // Am Heart J. 2000. Vol. 140. P. 878–885.
- Donal E., Lip G. Y., Galderisi M. et al. EACVI/EHRA Expert Consensus Document on the role of multi-modality imaging for the evaluation of patients with atrial fibrillation // Eur Heart J Cardiovasc Imaging. 2016. Vol. 17. P. 355–383.
- Lang R. M., Badano L. P., Mor-Avi V. et al. Recommendations for cardiac chamber quantification by echocardiography in adults: an update from the american society of echocardiography and the European association of cardiovascular imaging // Eur Heart J Cardiovasc Imaging. 2015. Vol. 16. P. 233–271.
- Cannon C. P., McCabe C. H., Stone P. H. et al. The electrocardiogram predicts one-year outcome of patients with unstable angina and non-Q wave myocardial infarction: Results of the TIMI III Registry ECG Ancillary Study // J Am Coll Cardiol. 1997. Vol. 30. P. 133–140.
- Savonitto S., Adrissino D., Gragner C. B. et al. Prognostic value of the admission electrocardiogram in acute coronary syndromes // JAMA. 1999. Vol. 281. P. 707–713.
- Thygesen K., Alpert J. S., Jaffe A. S. et al. Third universal definition of myocardial infarction // Am J Cardiol. 2012. Vol. 60, № 16. P. 1581–98.
- Метелев И. С., Соловьев О. В., Онучина Е. Л. и др. Диагностическая эффективность изменений ЭКГ и уровня тропонина в прогнозировании коронарного атеросклероза у пациентов с острым коронарным синдромом без подъема сегмента ST и острой фибрилляцией предсердий // Вятский медицинский вестник. 2017. Т. 3. № 55. С. 45–50.
- Al Khadir D., Alshengeiti L., Elbarouni B. et al. Management and outcome of acute coronary syndrome patients in relation to prior history of atrial fibrillation // Canadian Journal of Cardiology. 2012. Vol. 28. P. 443–449.
- Batra G., Svennblad B., Held C. et al. All Types of Atrial Fibrillation in the Setting of Myocardial Infarction are Associated with Impaired Outcome // Heart. 2016. Vol. 102. P. 926–933.
- Dai Y., Yang J., Gao Z. et al. Atrial Fibrillation in Patients Hospitalized with Acute Myocardial Infarction: Analysis of the China Acute Myocardial Infarction (CAMI) Registry // BMC Cardiovascular Disorders. 2017. Vol. 17. P. 2.
- Jabre P., Roger V., Murad M. et al. Mortality Associated with Atrial Fibrillation in Patients with Myocardial Infarction // Circulation. 2011. Vol. 123. P. 1587–1593.
И. С. Метелев1
О. В. Соловьев, доктор медицинских наук, профессор
Е. Л. Онучина, кандидат медицинских наук
С. К. Кононов, кандидат медицинских наук
ФГБОУ ВО Кировский ГМУ МЗ РФ, Киров
1 Контактная информация: rybanalim@rambler.ru
Ишемия миокарда на фоне пароксизма фибрилляции предсердий: прямое следствие аритмии или признак коронарного атеросклероза?/ И. С. Метелев, О. В. Соловьев, Е. Л. Онучина, С. К. Кононов
Для цитирования: Лечащий врач № 12/2018; Номера страниц в выпуске: 54-58
Теги: нарушения ритма сердца, предикторы, прогноз
Купить номер с этой статьей в pdf
Источник
